Lantus pro léčbu cukrovky
Název značky: Lantus
Obecný název: inzulín glargin
Dávková forma: Injekce (Lantus NESMÍ být naředěn nebo smíchán s jiným inzulinem nebo roztokem)
Obsah:
Popis
Klinická farmakologie
Indikace a použití
Kontraindikace
Varování
Opatření
Nežádoucí reakce
Dávkování a správa
Jak se dodává
Lantus, inzulín glargin (původ rDNA), informace o pacientech (v prosté angličtině)
Popis
Lantus® (injekce inzulínu glargin [rDNA původ]) je sterilní roztok inzulínu glargin pro použití jako injekce. Inzulín glargin je rekombinantní analog lidského inzulínu, který je dlouhodobě působící (až 24 hodinové působení), parenterální látka snižující krevní glukózu. (Vidět KLINICKÁ FARMAKOLOGIE). Lantus je produkován technologií rekombinantní DNA využívající nepatogenní laboratorní kmen Escherichia coli (K12) jako produkční organismus. Inzulín glargin se liší od lidského inzulínu v tom, že aminokyselina asparagin v poloze A21 je nahrazena glycinem a dva argininy jsou přidány na C-konec B-řetězce. Chemicky je to lidský inzulín 21A-Gly-30Ba-L-Arg-30Bb-L-Arg-lidský a má empirický vzorec C267H404N72O78S6 a molekulovou hmotnost 6063. Má následující strukturní vzorec:
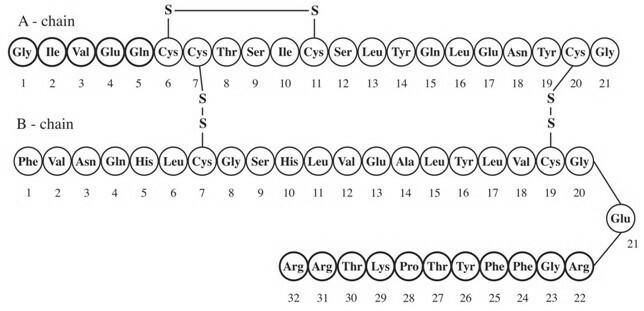
Lantus se skládá z inzulínu glargin rozpuštěného v čiré vodné tekutině. Každý mililiter přípravku Lantus (injekce inzulínu glargin) obsahuje 100 IU (3,6378 mg) inzulínu glargin.
Neaktivní přísady pro 10 ml lahvičku jsou 30 mcg zinku, 2,7 mg m-kresolu, 20 mg glycerolu 85%, 20 mcg polysorbátu 20 a voda pro injekce.
Neaktivní složky pro 3 ml patrony jsou 30 mcg zinku, 2,7 mg m-kresolu, 20 mg glycerolu 85% a voda pro injekce.
PH se upraví přidáním vodných roztoků kyseliny chlorovodíkové a hydroxidu sodného. Lantus má pH přibližně 4.
horní
Klinická farmakologie
Mechanismus účinku
Primární aktivita inzulínu, včetně inzulínu glargin, je regulace metabolismu glukózy. Inzulín a jeho analogy snižují hladiny glukózy v krvi stimulací periferní absorpce glukózy, zejména kosterního svalu a tuku, a inhibicí produkce glukózy v játrech. Inzulín inhibuje lipolýzu v adipocytu, inhibuje proteolýzu a zvyšuje syntézu proteinů.
Farmakodynamika
Inzulín glargin je analog lidského inzulínu, který byl navržen tak, aby měl nízkou rozpustnost ve vodě při neutrálním pH. Při pH 4 je stejně jako v injekčním roztoku Lantus zcela rozpustný. Po injekci do podkožní tkáně se kyselý roztok neutralizuje, což vede k tvorbě mikrosráženin, z nichž malé množství inzulínu glarginu se pomalu uvolňují, což vede k relativně konstantnímu profilu koncentrace / času po dobu 24 hodin bez výrazného vrchol. Tento profil umožňuje dávkování jednou denně jako bazální inzulín pacienta.
V klinických studiích je účinek na snížení hladiny glukózy na molární bázi (tj. Když je podáván ve stejných dávkách) intravenózního inzulínu glarginu přibližně stejný jako lidský inzulín. Ve studiích s euglykémií u zdravých jedinců nebo u pacientů s diabetem 1. typu byl nástup účinku subkutánního inzulínu glarginu pomalejší než lidský inzulín NPH. Profil účinku inzulínu glargin byl relativně konstantní bez výrazného píku a trvání jeho účinku bylo ve srovnání s lidským inzulínem NPH prodlouženo. Obrázek 1 ukazuje výsledky studie u pacientů s diabetem typu 1 prováděných po dobu maximálně 24 hodin po injekci. Střední doba mezi injekcí a koncem farmakologického účinku byla 14,5 hodin (rozmezí: 9,5 až 19,3 hodin) pro NPH lidský inzulín a 24 hodin (rozmezí: 10,8 až> 24,0 hodin) (24 hodin byl konec pozorovacího období) pro inzulin glargine.
Obrázek 1. Profil aktivity u pacientů s diabetem 1. typu
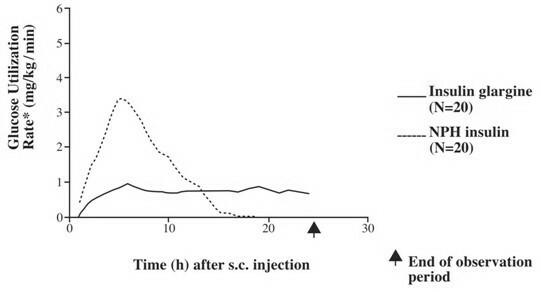
* Stanoveno jako množství infuze glukózy k udržení konstantních hladin glukózy v plazmě (hodinové průměrné hodnoty); svědčící o inzulínové aktivitě.
- variabilita mezi pacienty (CV, variační koeficient); inzulín glargin, 84% a NPH, 78%.
Delší doba působení (až 24 hodin) Lantusu přímo souvisí s jeho pomalejší absorpcí a podporuje subkutánní podání jednou denně. Časový průběh působení inzulínů, včetně Lantusu, se může lišit mezi jednotlivci a / nebo u stejného jedince.
Farmakokinetika
Absorpce a biologická dostupnost
Po subkutánní injekci inzulínu glargin u zdravých jedinců a pacientů s diabetem ukázaly koncentrace inzulínu v séru a pomalejší, delší prodloužení absorpce a relativně konstantní profil koncentrace / čas po dobu 24 hodin bez výrazného píku ve srovnání s NPH člověkem inzulín. Koncentrace inzulínu v séru byly tedy konzistentní s časovým profilem farmakodynamické aktivity inzulínu glargin.
Po subkutánní injekci 0,3 IU / kg inzulínu glargin u pacientů s diabetem typu 1 byl prokázán relativně konstantní profil koncentrace / čas. Trvání účinku po subkutánním podání v břiše, deltoidu nebo stehně bylo podobné.
Metabolismus
Studie metabolismu na lidech naznačuje, že inzulín glargin je částečně metabolizován na karboxylovém konci řetězce B v subkutánním depot za vzniku dvou aktivních metabolitů s in vitro aktivitou podobnou aktivitě inzulínu, M1 (21A-Gly-inzulín) a M2 (21A-Gly-des-30B-Thr-inzulín). V oběhu jsou také nezměněné léčivo a tyto degradační produkty.
Zvláštní populace
Věk, rasa a pohlaví
Informace o účinku věku, rasy a pohlaví na farmakokinetiku přípravku Lantus nejsou k dispozici. Avšak v kontrolovaných klinických studiích u dospělých (n = 3890) a v kontrolovaných klinických studiích u pediatrických pacientů (n = 349), podskupina analýzy založené na věku, rase a pohlaví neprokázaly rozdíly v bezpečnosti a účinnosti mezi inzulínem glargin a lidským NPH inzulín.
Kouření
Účinek kouření na farmakokinetiku / farmakodynamiku přípravku Lantus nebyl studován.
Těhotenství
Účinek těhotenství na farmakokinetiku a farmakodynamiku přípravku Lantus nebyl studován (viz OPATŘENÍ, Těhotenství).
Obezita
V kontrolovaných klinických studiích, které zahrnovaly pacienty s indexem tělesné hmotnosti (BMI) do 49,6 kg / m2 včetně, analýzy podskupin založené na BMI neprokázaly žádné rozdíly v bezpečnosti a účinnosti mezi inzulinem glarginem a lidským NPH inzulín.
Renální postižení
Účinek poškození ledvin na farmakokinetiku přípravku Lantus nebyl studován. Některé studie s lidským inzulínem však prokázaly zvýšené hladiny inzulinu v oběhu u pacientů se selháním ledvin. U pacientů s renální dysfunkcí může být nezbytné pečlivé sledování hladiny glukózy a úprava dávky inzulínu, včetně přípravku Lantus OPATŘENÍ, Renální postižení).
Jaterní postižení
Účinek poškození jater na farmakokinetiku přípravku Lantus nebyl studován. Některé studie s lidským inzulínem však prokázaly zvýšené hladiny cirkulujícího inzulínu u pacientů se selháním jater. U pacientů s jaterní dysfunkcí může být nezbytné pečlivé sledování hladiny glukózy a úprava dávky inzulínu, včetně přípravku Lantus OPATŘENÍ, Hepatální poškození).
Klinické studie
Bezpečnost a účinnost inzulínu glarginu podaného jednou denně před spaním byla porovnána s bezpečností a účinností lidského inzulínu NPH jednou denně a dvakrát denně v otevřeném, randomizovaném, aktivní kontrola, paralelní studie 2327 dospělých pacientů a 349 dětských pacientů s diabetes mellitus 1. typu a 1563 dospělých pacientů s diabetes mellitus 2. typu (viz tabulky) 1-3). Obecně byla redukce glykovaného hemoglobinu (HbA1c) Lantusem podobná jako u lidského inzulínu NPH. Celková míra hypoglykémie se nelišila mezi pacienty s diabetem léčeným Lantusem ve srovnání s lidským inzulínem NPH.
Diabetes typu 1 typu Adult (viz tabulka 1).
Ve dvou velkých, randomizovaných, kontrolovaných klinických studiích (studie A a B), pacienti s diabetem typu 1 (studie A; n = 585, studie B; n = 534) byly randomizovány na bazální bolusovou léčbu Lantusem jednou denně před spaním nebo na NPH lidský inzulín jednou nebo dvakrát denně a léčeny po dobu 28 týdnů. Před každým jídlem byl podáván normální lidský inzulín. Lantus byl podáván před spaním. Lidský inzulín NPH byl podáván jednou denně před spaním nebo ráno a před spaním, když byl použit dvakrát denně. V jedné velké, randomizované, kontrolované klinické studii (studie C), pacienti s diabetem 1. typu (n = 619) byly léčeny po dobu 16 týdnů bazálním bolusovým inzulinovým režimem, kde byl před každým použit inzulín lispro jídlo. Lantus byl podáván jednou denně před spaním a lidský inzulín NPH byl podáván jednou nebo dvakrát denně. V těchto studiích měl lidský inzulín Lantus a NPH podobný účinek na glykohemoglobin s podobnou celkovou mírou hypoglykémie.
Tabulka 1: Diabetes typu 1 Mellitus-Adult
| Studie A | Studie B | Studie C | ||||
|---|---|---|---|---|---|---|
| Délka léčby | 28 týdnů | 28 týdnů | 16 týdnů | |||
| Léčba v kombinaci s | Běžný inzulín | Běžný inzulín | Inzulín lispro | |||
| Lantus | NPH | Lantus | NPH | Lantus | NPH | |
| Počet léčených subjektů | 292 | 293 | 264 | 270 | 310 | 309 |
| HbA1c | ||||||
| Endstudy znamená | 8.13 | 8.07 | 7.55 | 7.49 | 7.53 | 7.60 |
| Adj. průměrná změna oproti základní hodnotě | +0.21 | +0.10 | -0.16 | -0.21 | -0.07 | -0.08 |
| Lantus - NPH | +0.11 | +0.05 | +0.01 | |||
| 95% CI pro rozdíl v léčbě | (-0.03; +0.24) | (-0.08; +0.19) | (-0.11; +0.13) | |||
| Bazální dávka inzulínu | ||||||
| Endstudy znamená | 19.2 | 22.8 | 24.8 | 31.3 | 23.9 | 29.2 |
| Průměrná změna oproti základní linii | -1.7 | -0.3 | -4.1 | +1.8 | -4.5 | +0.9 |
| Celková dávka inzulínu | ||||||
| Endstudy znamená | 46.7 | 51.7 | 50.3 | 54.8 | 47.4 | 50.7 |
| Průměrná změna oproti základní linii | -1.1 | -0.1 | +0.3 | +3.7 | -2.9 | +0.3 |
| Hladina glukózy v krvi nalačno (mg / dl) | ||||||
| Endstudy znamená | 146.3 | 150.8 | 147.8 | 154.4 | 144.4 | 161.3 |
| Adj. průměrná změna oproti základní hodnotě | -21.1 | -16.0 | -20.2 | -16.9 | -29.3 | -11.9 |
Diabetes typu 1 pro děti (viz tabulka 2).
V randomizované, kontrolované klinické studii (studie D), dětští pacienti (věkové rozmezí 6 až 15 let) s diabetem 1. typu (n = 349) byly léčeny po dobu 28 týdnů bazálním bolusovým inzulinovým režimem, kde byl před každým běžným lidským inzulínem použit jídlo. Lantus byl podáván jednou denně před spaním a lidský inzulín NPH byl podáván jednou nebo dvakrát denně. Podobné účinky na glykohemoglobin a výskyt hypoglykémie byly pozorovány v obou léčených skupinách.
Tabulka 2: Diabetes typu 1 Mellitus-Pediatric
| Studie D | ||
|---|---|---|
| Délka léčby | 28 týdnů | |
| Léčba v kombinaci s | Běžný inzulín | |
| Lantus | NPH | |
| Počet léčených subjektů | 174 | 175 |
| HbA1c | ||
| Endstudy znamená | 8.91 | 9.18 |
| Adj. průměrná změna oproti základní hodnotě | +0.28 | +0.27 |
| Lantus - NPH | +0.01 | |
| 95% CI pro rozdíl v léčbě | (-0.24; +0.26) | |
| Bazální dávka inzulínu | ||
| Endstudy znamená | 18.2 | 21.1 |
| Průměrná změna oproti základní linii | -1.3 | +2.4 |
| Celková dávka inzulínu | ||
| Endstudy znamená | 45.0 | 46.0 |
| Průměrná změna oproti základní linii | +1.9 | +3.4 |
| Hladina glukózy v krvi nalačno (mg / dl) | ||
| Endstudy znamená | 171.9 | 182.7 |
| Adj. průměrná změna oproti základní hodnotě | -23.2 | -12.2 |
Diabetes 2. typu (viz tabulka 3).
Ve velké, randomizované, kontrolované klinické studii (studie E) (n = 570) byl Lantus hodnocen po dobu 52 týdnů jako součást režimu kombinovaná terapie s inzulínem a perorálními antidiabetiky (sulfonylmočovina, metformin, akarbóza nebo jejich kombinace drogy). Lantus podávaný jednou denně před spaním byl stejně účinný jako lidský inzulín NPH podávaný jednou denně před spaním při snižování glykohemoglobinu a glukózy nalačno. U pacientů léčených lidským inzulínem Lantus a NPH byla nízká míra hypoglykémie. Ve velké, randomizované, kontrolované klinické studii (studie F) u pacientů s diabetem 2. typu, kteří nepoužívají perorální antidiabetika (n = 518), bazální bolusový režim Lantusu jednou denně před spaním nebo NPH lidský inzulín podávaný jednou nebo dvakrát denně byl hodnocen na 28 týdnů. Před jídlem byl podle potřeby používán běžný lidský inzulín. Lantus měl při snižování glykohemoglobinu a glukózy na lačno s podobným výskytem hypoglykémie podobnou účinnost jako lidský inzulín NPH jednou nebo dvakrát denně.
Tabulka 3: Diabetes typu 2 Mellitus-Adult
| Studie E | Studie F | |||
|---|---|---|---|---|
| Délka léčby | 52 týdnů | 28 týdnů | ||
| Léčba v kombinaci s | Orální agenti | Běžný inzulín | ||
| Lantus | NPH | Lantus | NPH | |
| Počet léčených subjektů | 289 | 281 | 259 | 259 |
| HbA1c | ||||
| Endstudy znamená | 8.51 | 8.47 | 8.14 | 7.96 |
| Adj. průměrná změna oproti základní hodnotě | -0.46 | -0.38 | -0.41 | -0.59 |
| Lantus - NPH | -0.08 | +0.17 | ||
| 95% CI pro rozdíl v léčbě | (-0.28; +0.12) | (-0.00; +0.35) | ||
| Bazální dávka inzulínu | ||||
| Endstudy znamená | 25.9 | 23.6 | 42.9 | 52.5 |
| Průměrná změna oproti základní linii | +11.5 | +9.0 | -1.2 | +7.0 |
| Celková dávka inzulínu | ||||
| Endstudy znamená | 25.9 | 23.6 | 74.3 | 80.0 |
| Průměrná změna oproti základní linii | +11.5 | +9.0 | +10.0 | +13.1 |
| Hladina glukózy v krvi nalačno (mg / dl) | ||||
| Endstudy znamená | 126.9 | 129.4 | 141.5 | 144.5 |
| Adj. průměrná změna oproti základní hodnotě | -49.0 | -46.3 | -23.8 | -21.6 |
Flexibilní denní dávkování Lantus
Bezpečnost a účinnost přípravku Lantus podávaného před snídaní, před večeří nebo před spaním byla hodnoceno ve velké, randomizované, kontrolované klinické studii u pacientů s diabetem 1. typu (studie G, n = 378). Pacienti byli také léčeni inzulínem lispro v době jídla. Lantus podávaný v různých denních dobách měl za následek podobné snížení glykovaného hemoglobinu ve srovnání s podáváním před spaním (viz tabulka 4). U těchto pacientů jsou k dispozici data z 8bodového domácího sledování hladiny glukózy. Maximální průměrná hladina glukózy v krvi byla pozorována těsně před injekcí Lantusu bez ohledu na čas podání, tj. Před snídaní, před večeří nebo před spaním.
V této studii 5% pacientů v rameni Lantus se snídaní přerušilo léčbu z důvodu nedostatečné účinnosti. Žádní pacienti ve zbývajících dvou ramenech z tohoto důvodu neskončili. Rutinní monitorování během této studie odhalilo následující průměrné změny systolického krevního tlaku: skupina před snídaní, 1,9 mm Hg; skupina před večeří, 0,7 mm Hg; skupina před spaním, -2,0 mm Hg.
Bezpečnost a účinnost přípravku Lantus podávaného před snídaní nebo před spaním byla také hodnocena ve velkém, náhodném pořadí, aktivní kontrolovaná klinická studie (Studie H, n = 697) u pacientů s diabetem 2. typu, kteří již nejsou dostatečně kontrolováni perorálním agens terapie. Všichni pacienti v této studii také dostávali AMARYL® (glimepirid) 3 mg denně. Lantus podávaný před snídaní byl přinejmenším stejně účinný při snižování glykovaného hemoglobinu A1c (HbA1c) jako Lantus podávaný před spaním nebo NPH lidský inzulín podávaný před spaním (viz tabulka 4).
Tabulka 4: Flexibilní denní dávkování Lantusu u diabetu Mellitus typu 1 (studie G) a typu 2 (studie H)
| Studie G | Studium H. | |||||
|---|---|---|---|---|---|---|
| Léčbadurace | 24 týdnů | 24 týdnů | ||||
| Ošetření v kombinaci s: | Inzulín lispro | AMARYL® (glimepirid) | ||||
| Lantus Snídaně |
Lantus Večeře |
Lantus Před spaním |
Lantus Snídaně |
Lantus Před spaním |
NPH Před spaním |
|
| ||||||
| Počet léčených subjektů* | 112 | 124 | 128 | 234 | 226 | 227 |
| HbA1c | ||||||
| Střední hodnota | 7.56 | 7.53 | 7.61 | 9.13 | 9.07 | 9.09 |
| Endstudy znamená | 7.39 | 7.42 | 7.57 | 7.87 | 8.12 | 8.27 |
| Průměrná změna oproti základní linii | -0.17 | -0.11 | -0.04 | -1.26 | -0.95 | -0.83 |
| Bazální dávka inzulínu (IU) | ||||||
| Endstudy znamená | 27.3 | 24.6 | 22.8 | 40.4 | 38.5 | 36.8 |
| Průměrná změna oproti základní linii | 5.0 | 1.8 | 1.5 | |||
| Celková dávka inzulínu (IU) | NAâ € | NA | NA | |||
| Endstudy znamená | 53.3 | 54.7 | 51.5 | |||
| Průměrná změna oproti základní linii | 1.6 | 3.0 | 2.3 |
horní
Indikace a použití
Lantus je indikován k subkutánnímu podání jednou denně k léčbě dospělých a pediatrických pacientů s typem 1 diabetes mellitus nebo dospělí pacienti s diabetes mellitus 2. typu, kteří vyžadují bazální (dlouhodobě působící) inzulín pro kontrolu hyperglykémie.
horní
Kontraindikace
Přípravek Lantus je kontraindikován u pacientů s přecitlivělostí na inzulín glargin nebo na pomocné látky.
horní
Varování
Hypoglykémie je nejčastějším nepříznivým účinkem inzulínu, včetně Lantusu. Stejně jako u všech inzulínů se načasování hypoglykémie může u různých inzulínových přípravků lišit. Monitorování glukózy se doporučuje všem pacientům s diabetem.
Jakákoli změna inzulinu by měla být prováděna opatrně a pouze pod lékařským dohledem. Změny síly inzulínu, načasování dávkování, výrobce, typ (např. Normální, NPH nebo analogy inzulínu), druh (zvíře, lidský) nebo způsob výroby (rekombinantní DNA versus živočišný zdroj inzulínu) může vést k potřebě změny v dávkování. Může být nutné upravit současnou orální antidiabetickou léčbu.
horní
Opatření
Všeobecné
Lantus není určen k intravenóznímu podání. Prodloužené trvání aktivity inzulínu glargin závisí na injekci do podkožní tkáně. Intravenózní podání obvyklé subkutánní dávky může vést k těžké hypoglykémii.
Lantus NESMÍ být naředěn nebo smíchán s jiným inzulinem nebo roztokem. Pokud je přípravek Lantus naředěn nebo smíchán, může dojít k zakalení roztoku a farmakokinetickému / farmakodynamickému profilu (např. nástup účinku, doba do dosažení maximálního účinku) Lantusu a / nebo smíšeného inzulínu může být změněn v nepředvídatelné způsob. Když byly Lantus a běžný lidský inzulín smíchány bezprostředně před injekcí u psů, byl pozorován opožděný nástup účinku a čas do maximálního účinku na normální lidský inzulín. Celková biologická dostupnost směsi byla také mírně snížena ve srovnání se samostatnými injekcemi Lantusu a běžného lidského inzulínu. Význam těchto pozorování u psů u lidí není znám.
Stejně jako u všech inzulínových přípravků se časový průběh účinku Lantusu může u různých jedinců lišit časy u stejného jednotlivce a rychlost absorpce závisí na krevním zásobení, teplotě a fyzickém stavu aktivita.
Inzulín může způsobit retenci sodíku a otoky, zejména pokud se dříve zeslabená metabolická kontrola zlepší intenzivní inzulinovou terapií.
Hypoglykémie
Stejně jako u všech inzulínových přípravků může být s podáváním přípravku Lantus spojena hypoglykemická reakce. Hypoglykémie je nejčastějším nepříznivým účinkem inzulínů. Včasné varovné příznaky hypoglykémie se mohou za určitých podmínek, například dlouhé, lišit trvání diabetu, onemocnění diabetických nervů, použití léků, jako jsou beta-blokátory, nebo zesílená kontrola diabetu (vidět OPATŘENÍ, Lékové interakce). Takové situace mohou vést k těžké hypoglykémii (a možná ke ztrátě vědomí) před tím, než si pacient uvědomí hypoglykémii.
Čas výskytu hypoglykémie závisí na profilu účinku použitých inzulínů, a proto se může změnit, když se změní léčebný režim nebo načasování dávkování. Pacienti, kteří přecházejí z inzulínu NPH dvakrát denně na Lantus jednou denně, by měli mít počáteční dávku Dávka Lantusu se snížila o 20% z předchozí celkové denní dávky NPH, aby se snížilo riziko hypoglykémie (vidět DÁVKOVÁNÍ A PODÁNÍ, Přechod na Lantus).
Prodloužený účinek subkutánního Lantusu může oddálit zotavení z hypoglykémie.
V klinické studii byly příznaky hypoglykémie nebo odezvy kontraregulačních hormonů podobné intravenózní inzulín glargin a normální lidský inzulín u zdravých jedinců iu pacientů s typem 1 cukrovka.
Renální postižení
Ačkoli studie nebyly provedeny u pacientů s cukrovkou a poškozením ledvin, požadavky na Lantus může být snížena kvůli sníženému metabolismu inzulínu, podobně jako u jiných inzulínů (vidět KLINICKÁ FARMAKOLOGIE, Zvláštní populace).
Jaterní postižení
Přestože studie u pacientů s cukrovkou a jaterním poškozením nebyly provedeny, mohou být požadavky na Lantus sníženy kvůli snížené kapacitě pro glukoneogenezi a sníženému metabolismu inzulínu, podobné pozorováním zjištěným u jiných inzulínů (viz KLINICKÁ FARMAKOLOGIE, Zvláštní populace).
Místo vpichu a alergické reakce
Stejně jako u každé inzulínové terapie se v místě vpichu může objevit lipodystrofie a zpomalit absorpci inzulínu. Mezi další reakce v místě vpichu s inzulinovou terapií patří zarudnutí, bolest, svědění, kopřivka, otok a zánět. Neustálé střídání místa vpichu v dané oblasti může pomoci zmírnit nebo zabránit těmto reakcím. Většina menších reakcí na inzulíny obvykle ustoupí za několik dní až týdnů.
Zprávy o bolesti v místě vpichu byly častější u přípravku Lantus než u lidského inzulinu NPH (2,7% inzulínu glargin oproti 0,7% NPH). Zprávy o bolesti v místě vpichu byly obvykle mírné a neměly za následek přerušení léčby.
Alergické reakce bezprostředního typu jsou vzácné. Takové reakce na inzulín (včetně inzulínu glargin) nebo pomocné látky mohou být například spojeny s generalizovanými kožními reakcemi, angioedémem, bronchospasmem, hypotenzí nebo šokem a může to být život hrozivý.
Interkurentní podmínky
Požadavky na inzulín mohou být změněny během interkurentních stavů, jako jsou nemoci, emoční poruchy nebo stres.
Informace pro pacienty
Lantus se smí použít pouze tehdy, je-li roztok čirý a bezbarvý bez viditelných částic (viz DÁVKOVÁNÍ A PODÁNÍ, Příprava a manipulace).
Pacienti musí být upozorněni, že Lantus NESMÍ být ředěn nebo míchán s jakýmkoli jiným inzulinem nebo roztokem (viz OPATŘENÍ, Všeobecné).
Pacienti by měli být poučeni o postupech samosprávy, včetně monitorování glukózy, správné techniky injekce a hypoglykémie a hyperglykémie. Pacienti musí být poučeni o řešení zvláštních situací, jako jsou interkurentní stavy (nemoc, stres nebo emoční) poruchy), nepřiměřená nebo přeskočená dávka inzulínu, neúmyslné podání zvýšené dávky inzulínu, nedostatečný příjem potravy nebo vynechaná jídla. Další informace najdete v kruhovém „Informace o pacientovi“ Lantus.
Stejně jako u všech pacientů s diabetem může být schopnost koncentrace a / nebo reakce snížena v důsledku hypoglykémie nebo hyperglykémie.
Pacientky s diabetem by měly být informovány, aby informovaly svého zdravotnického pracovníka, pokud jsou těhotné nebo uvažují o těhotenství.
Lékové interakce
Řada látek ovlivňuje metabolismus glukózy a může vyžadovat úpravu dávky inzulínu a zvláště pečlivé sledování.
Následuje příklad látek, které mohou zvýšit účinek na snížení hladiny glukózy v krvi a náchylnost k hypoglykémii: perorální antidiabetika, ACE inhibitory, disopyramid, fibráty, fluoxetin, MAO inhibitory, propoxyfen, salicyláty, analog somatostatinu (např. Oktreotid), sulfonamid antibiotika.
Následuje příklad látek, které mohou snižovat účinek inzulinu na snižování hladiny glukózy v krvi: kortikosteroidy, danazol, diuretika, sympatomimetika (např. epinefrin, albuterol, terbutalin), isoniazid, deriváty fenothiazinu, somatropin, hormony štítné žlázy, estrogeny, progestogeny (např. v perorální antikoncepci), inhibitory proteázy a atypická antipsychotika (např. olanzapin a clozapin).
Beta-blokátory, klonidin, lithné soli a alkohol mohou buď zesílit nebo oslabit účinek inzulínu na snížení hladiny glukózy v krvi. Pentamidin může způsobit hypoglykémii, po které může někdy následovat hyperglykémie.
Kromě toho mohou být pod vlivem sympatolytických léčivých přípravků, jako jsou beta-blokátory, klonidin, guanethidin a reserpin, známky hypoglykémie sníženy nebo chybí.
Karcinogeneze, mutageneze, zhoršení plodnosti
U myší a potkanů byly provedeny standardní dvouleté studie karcinogenity s inzulinem glargin v dávkách až 0,455 mg / kg, což je pro potkan přibližně 10krát a pro myš přibližně 5násobek doporučené lidské podkožní počáteční dávky 10 IU (0,008 mg / kg / den), vztaženo na mg / m2. Nálezy u samic myší nebyly přesvědčivé kvůli nadměrné úmrtnosti ve všech dávkových skupinách během studie. Histiocytomy byly nalezeny v místě injekce u samců potkanů (statisticky významné) a samců myší (ne statisticky významných) ve skupinách obsahujících kyselé vehikulum. Tyto nádory nebyly nalezeny u samic, u fyziologického roztoku nebo u srovnávacích skupin inzulínu pomocí jiného vehikula. Význam těchto zjištění pro člověka není znám.
Inzulín glargin nebyl mutagenní při testech na detekci genových mutací v bakteriích a savčích buňkách (Ames a HGPRT-test) a v testech pro detekci chromozomálních aberací (cytogenetika in vitro v buňkách V79 a in vivo v čínštině křečci).
V kombinované studii plodnosti a prenatální a postnatální studie u samců a samic potkanů v subkutánních dávkách až do 0,36 mg / kg / den, což je přibližně 7násobek doporučená počáteční subkutánní dávka u člověka 10 IU (0,008 mg / kg / den), založená na mg / m2, mateřské toxicitě v důsledku hypoglykémie závislé na dávce, včetně některých úmrtí, byla pozorováno. V důsledku toho došlo ke snížení rychlosti chovu pouze ve skupině s vysokou dávkou. Podobné účinky byly pozorovány u lidského inzulinu NPH.
Těhotenství
Teratogenní účinky
Kategorie těhotenství C. Byly provedeny subkutánní reprodukční a teratologické studie s inzulínem glargin a běžným lidským inzulínem u potkanů a himálajských králíků. Lék byl podáván samicím krys před pářením, během páření a během těhotenství v dávkách až 0,36 mg / kg / den, což je přibližně 7krát větší než doporučená počáteční subkutánní dávka u člověka 10 IU (0,008 mg / kg / den), vztaženo na mg / m2. U králíků dávka 0,072 mg / kg / den, což je přibližně dvojnásobek doporučené dávky u člověka během subkutánní počáteční dávky 10 IU (0,008 mg / kg / den), vztaženo na mg / m2 organogeneze. Účinky inzulínu glargin se obecně nelišily od účinků pozorovaných u běžného lidského inzulínu u potkanů nebo králíků. U králíků však pět plodů ze dvou vrhů skupiny s vysokou dávkou vykazovalo dilataci mozkových komor. Plodnost a časný embryonální vývoj se zdály normální.
Neexistují žádné dobře kontrolované klinické studie o používání inzulínu glargin u těhotných žen. Pro pacienty s diabetem nebo s gestačním diabetem v anamnéze je nezbytné udržovat dobrou metabolickou kontrolu před početí a během těhotenství. Požadavky na inzulín se mohou během prvního trimestru snižovat, obvykle se zvyšují během druhého a třetího trimestru a po porodu rychle klesají. U těchto pacientů je nezbytné pečlivé sledování hladiny glukózy. Protože studie reprodukce na zvířatech ne vždy predikují lidskou odpověď, mělo by být toto léčivo použito během těhotenství, pouze pokud je to nezbytně nutné.
Kojící matky
Není známo, zda se inzulín glargin vylučuje ve významném množství do mateřského mléka. Mnoho léků, včetně lidského inzulínu, se vylučuje do mateřského mléka. Z tohoto důvodu je třeba při podávání přípravku Lantus kojící ženě postupovat opatrně. Kojící ženy mohou vyžadovat úpravu dávky inzulínu a stravy.
Pediatrické použití
Bezpečnost a účinnost přípravku Lantus byla stanovena ve věkové skupině 6 až 15 let s diabetem 1. typu.
Geriatrické použití
V kontrolovaných klinických studiích srovnávajících inzulín glargin s lidským inzulínem NPH bylo 593 z 3890 pacientů s diabetem typu 1 a typu 2 65 let a starších. Jediný rozdíl v bezpečnosti nebo účinnosti v této subpopulaci ve srovnání s celou populací studie byl očekávaný vyšší výskyt kardiovaskulárních příhod jak u inzulínu glargin, tak u NPH léčeného lidským inzulínem pacientů.
U starších pacientů s diabetem by mělo být počáteční dávkování, zvyšování dávky a udržovací dávka konzervativní, aby se zabránilo hypoglykemickým reakcím. U starších lidí může být obtížné rozpoznat hypoglykémii (viz OPATŘENÍ, Hypoglykémie).
horní
Nežádoucí reakce
Mezi nežádoucí příhody, které jsou běžně spojeny s přípravkem Lantus, patří následující:
Tělo jako celek: alergické reakce (viz OPATŘENÍ).
Kůže a přívěsky: reakce v místě vpichu, lipodystrofie, svědění, vyrážka (viz OPATŘENÍ).
Jiné: hypoglykémie (viz VAROVÁNÍ a OPATŘENÍ).
V klinických studiích u dospělých pacientů byl u pacientů léčených přípravkem Lantus vyšší výskyt bolesti v místě vpichu, který se objevil při léčbě (2,7%), ve srovnání s pacienty léčenými NPH inzulínem (0,7%). Zprávy o bolesti v místě vpichu byly obvykle mírné a neměly za následek přerušení léčby. Další reakce v místě vpichu, které se objevily při injekci, se objevily při podobné incidenci jak u inzulínu glarginu, tak u lidského inzulínu NPH.
Retinopatie byla hodnocena v klinických studiích pomocí zaznamenaných nežádoucích účinků sítnice a fotografováním fundusu. Počty retinálních nežádoucích účinků hlášených u léčených skupin Lantus a NPH byly podobné u pacientů s diabetem 1. a 2. typu. Průběh retinopatie byl zkoumán pomocí fundusové fotografie s použitím klasifikačního protokolu odvozeného ze studie včasné léčby diabetické retinopatie (ETDRS). V jedné klinické studii zahrnující pacienty s diabetem typu 2 je rozdíl v počtu subjektů s 3-krokem progresi v měřítku ETDRS v 6měsíčním období bylo zaznamenáno pomocí fundus fotografie (7,5% ve skupině Lantus versus 2,7% v NPH) ošetřená skupina). Celkový význam tohoto izolovaného nálezu nelze určit kvůli malému počtu pacientů a krátká doba sledování a skutečnost, že tento nález nebyl pozorován v jiných klinických studiích studie.
horní
Předávkovat
Nadbytek inzulínu vzhledem k příjmu potravy, energetickým výdajům nebo obojím může vést k těžké a někdy dlouhodobé a život ohrožující hypoglykémii. Mírné epizody hypoglykémie lze obvykle léčit perorálními uhlohydráty. Může být nutné upravit dávkování léků, vzorce jídla nebo cvičení.
Závažnější epizody s kómou, křečemi nebo neurologickým poškozením mohou být léčeny intramuskulárním / subkutánním glukagonem nebo koncentrovanou intravenózní glukózou. Po zjevném klinickém zotavení z hypoglykémie může být nezbytné další pozorování a další příjem uhlohydrátů, aby nedošlo k opětovnému výskytu hypoglykémie.
horní
Dávkování a správa
Lantus je rekombinantní analog lidského inzulínu. Jeho účinnost je přibližně stejná jako u lidského inzulínu. Vykazuje relativně konstantní profil snižování glukózy po dobu 24 hodin, který umožňuje dávkování jednou denně.
Lantus lze podávat kdykoli během dne. Lantus by měl být podáván subkutánně jednou denně ve stejnou dobu každý den. Informace o pacientech, kteří upravují načasování dávkování přípravkem Lantus, viz VAROVÁNÍ a OPATŘENÍ, Hypoglykémie. Lantus není určen k intravenóznímu podání (viz OPATŘENÍ). Intravenózní podání obvyklé subkutánní dávky může vést k těžké hypoglykémii. Požadované hladiny glukózy v krvi, jakož i dávky a načasování léků proti cukrovce musí být stanoveny individuálně. Monitorování hladiny glukózy v krvi se doporučuje všem pacientům s diabetem. Prodloužené trvání aktivity Lantusu závisí na injekci do podkožního prostoru.
Stejně jako u všech inzulínů se musí místo vpichu v oblasti injekce (břicho, stehno nebo deltoid) střídat z jedné injekce na druhou.
V klinických studiích nebyl žádný významný rozdíl v absorpci inzulínu glarginu po subkutánním podání břicha, deltoidu nebo stehna. Stejně jako u všech inzulínů může být rychlost absorpce a následně i nástup a trvání účinku ovlivněna cvičením a jinými proměnnými.
Lantus není inzulín volby pro léčbu diabetické ketoacidózy. Upřednostňovanou léčbou je intravenózní krátkodobě působící inzulín.
Pediatrické použití
Lantus lze bezpečně podávat dětským pacientům ve věku 6 let. Podávání dětským pacientům
Zahájení terapie Lantusem
V klinické studii s dosud neléčenými pacienty s inzulinem typu 2, kteří již byli léčeni perorálními antidiabetiky, byl přípravek Lantus zahájen průměrná dávka 10 IU jednou denně a následně upravená podle potřeby pacienta na celkovou denní dávku v rozmezí 2 až 100 IU.
Přechod na Lantus
Pokud se změní z léčebného režimu střednědobým nebo dlouhodobě působícím inzulínem na režim s Lantusem, množství a načasování krátkodobě působícího inzulínu nebo rychle působícího inzulínového analogu nebo dávky jakéhokoli perorálního antidiabetika může být nutné upraveno. V klinických studiích, kdy byli pacienti převedeni z lidského inzulínu NPH nebo ultralente lidského inzulinu na Lantus jednou denně, se počáteční dávka obvykle nezměnila. Když však byli pacienti převedeni z lidského inzulínu NPH dvakrát denně na Lantus jednou denně, aby se snížilo riziko hypoglykémie, počáteční dávka (IU) byla obvykle snížena přibližně o 20% (ve srovnání s celkovou denní IU lidského inzulínu NPH) a poté upravena na základě reakce pacienta (vidět OPATŘENÍ, Hypoglykémie).
Během přenosu a v prvních týdnech po něm se doporučuje pečlivé sledování metabolismu pod lékařským dohledem. Může být nutné upravit množství a načasování krátkodobě působícího inzulínu nebo rychle působícího inzulínového analogu. To platí zejména pro pacienty se získanými protilátkami proti lidskému inzulinu, kteří potřebují vysoké dávky inzulínu, a vyskytuje se u všech analogů inzulínu. Může být nutné upravit dávku Lantusu a dalších inzulínů nebo perorálních antidiabetik; například pokud načasování dávkování pacienta, změna hmotnosti nebo životního stylu nebo jiné okolnosti, které zvyšují náchylnost k hypoglykémii nebo hyperglykémii (viz OPATŘENÍ, Hypoglykémie).
Dávka může být také nutné upravit během interkurentního onemocnění (viz OPATŘENÍ, Interkurentní podmínky).
Příprava a manipulace
Parenterální léčivé přípravky by měly být před podáním vizuálně zkontrolovány, kdykoli to roztok a nádoba dovolí. Lantus se smí použít pouze tehdy, je-li roztok čirý a bezbarvý bez viditelných částic.
Míchání a ředění: Lantus NESMÍ být ředěn nebo míchán s jakýmkoli jiným inzulinem nebo roztokem (viz OPATŘENÍ, Všeobecné).
Injekční lahvička: Injekční stříkačky nesmí obsahovat žádný jiný léčivý přípravek nebo zbytky.
Náplňový systém: Pokud OptiClik®, zařízení pro dodávání inzulínu pro Lantus, poruchy, může být Lantus natažen ze systému náplně do stříkačky U-100 a injikován.
horní
Jak se dodává
Lantus 100 jednotek na ml (U-100) je k dispozici v následující velikosti balení:
10 ml lahvičky (NDC 0088-2220-33)
3 ml náplňový systém1, balení 5 (NDC 0088-2220-52)
1Cartridge systémy jsou určeny pouze pro použití v OptiClik® (Insulin Delivery Device)
Úložný prostor
Neotevřený systém lahviček / patron
Neotevřené lahvičky a systémy s náplní Lantus by měly být uchovávány v chladničce (2 ° C - 8 ° C). Lantus by neměl být uchováván v mrazničce a nemělo by se nechat zmrznout.
Zlikvidujte, pokud byl zmrazený.
Otevřete (v provozu) systém lahviček / kazet
Otevřené injekční lahvičky, ať už chlazené nebo ne chlazené, musí být použity do 28 dnů po prvním použití. Pokud se nepoužijí do 28 dnů, musí být zlikvidovány. Pokud není možné chlazení, může být otevřená injekční lahvička ponechána bez chladničky po dobu až 28 dnů od přímého tepla a světla, dokud není teplota vyšší než 30 ° C.
Otevřený (v provozu) zásobníkový systém v OptiClik® NESMÍ být chlazený, ale měl by být uchováván při pokojové teplotě (do 30 ° C) mimo přímé teplo a světlo. Otevřený (v provozu) systém náplní v OptiClik® uchovávaný při pokojové teplotě musí být po 28 dnech zlikvidován. Neskladujte OptiClik®, ať už se zásobníkem nebo bez něj, v chladničce.
Lantus by neměl být uchováván v mrazničce a nemělo by se nechat zmrznout. Zlikvidujte, pokud byl zmrazený.
Tyto podmínky skladování jsou shrnuty v následující tabulce:
| Nepoužívaný (neotevřený) Chlazené |
Nepoužívaný (neotevřený) Pokojová teplota |
Při použití (otevřeno) (Viz Teplota níže) |
|
|---|---|---|---|
| 10 ml lahvička | Do data vypršení platnosti | 28 dní | 28 dní Chlazená nebo pokojová teplota |
| 3 ml Cartridge systém | Do data vypršení platnosti | 28 dní | 28 dní Chlazená nebo pokojová teplota |
| 3 ml kazeta systém vložen do OptiClik® |
28 dní Pouze pokojová teplota (Chraňte před chladem) |
Vyrobeno pro distribuci:
sanofi-aventis US LLC
Bridgewater NJ 08807
Vyrobeno v Německu
www. Lantus.com
© 2006 sanofi-aventis US LLC
OptiClik® je registrovaná ochranná známka společnosti sanofi-aventis U.S. LLC, Bridgewater NJ 08807
naposledy aktualizováno 04/2006
Lantus, inzulín glargin (původ rDNA), informace o pacientech (v prosté angličtině)
Podrobné informace o příznacích, příznacích, příčinách, léčbě cukrovky
Účelem informací v této monografii není pokrýt všechna možná použití, pokyny, preventivní opatření, lékové interakce nebo nepříznivé účinky. Tyto informace jsou zobecněné a neslouží jako zvláštní lékařská pomoc. Máte-li dotazy týkající se léků, které užíváte, nebo byste chtěli získat více informací, obraťte se na svého lékaře, lékárníka nebo zdravotní sestru.
zpět k: Procházet všechny léky na cukrovku


