Levemir pro léčbu cukrovky
Název značky: Levemir
Obecný název: Insulin Detemir
Dávková forma: injekce
Obsah:
Popis
Klinická farmakologie
Klinické studie
Indikace a použití
Kontraindikace
Varování
Opatření
Nežádoucí reakce
Předávkování
Dávkování a správa
Jak dodáván
Levemir, inzulin detemir (původ rDNA), informace o pacientech (v prosté angličtině)
Popis
Levemir® (injekce inzulínu detemiru [rDNA původ]) je sterilní roztok inzulínu detemiru pro použití jako injekce. Inzulin detemir je dlouhodobě působící bazální inzulinový analog s účinkem až 24 hodin, produkovaný a Tento proces zahrnuje expresi rekombinantní DNA v Saccharomyces cerevisiae následovanou chemickou látkou modifikace.
Inzulín detemir se liší od lidského inzulínu v tom, že aminokyselina threonin v poloze B30 byla vynechána a řetězec mastných kyselin C14 byl připojen k aminokyselině B29. Inzulin detemir má molekulový vzorec C267H402O76N64S6 a molekulovou hmotnost 5916,9. Má následující strukturu:
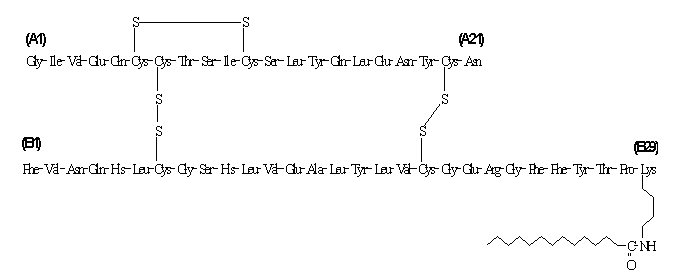
Levemir je čirý, bezbarvý, vodný, neutrální sterilní roztok. Každý mililitr Levemiru obsahuje 100 U (14,2 mg / ml) detemiru. Každý mililitr lahvičky s 10 ml Levemiru obsahuje inaktivní složky 65,4 mcg zinku, 2,06 mg m-kresolu, 30,0 mg mannitol, 1,80 mg fenolu, 0,89 mg dihydrátu hydrogenfosforečnanu sodného, 1,17 mg chloridu sodného a voda pro injekce. Každý mililitr náplně Levemir 3 ml PenFill®, FlexPen® a InnoLet® obsahuje neaktivní složky 65,4 mcg zinku, 2,06 mg m-kresol, 16,0 mg glycerolu, 1,80 mg fenolu, 0,89 mg dihydrátu hydrogenfosforečnanu sodného, 1,17 mg chloridu sodného a voda pro injekce. K úpravě pH lze přidat kyselinu chlorovodíkovou a / nebo hydroxid sodný. Levemir má pH přibližně 7,4.
horní
Klinická farmakologie
Mechanismus účinku
Primární aktivita inzulínu detemiru je regulace metabolismu glukózy. Inzuliny, včetně inzulínu detemir, projevují svůj specifický účinek prostřednictvím vazby na inzulínové receptory.
Inzulín vázaný inzulín snižuje hladinu glukózy v krvi tím, že usnadňuje buněčný příjem glukózy do kosterního svalu a tuku a inhibuje produkci glukózy z jater. Inzulín inhibuje lipolýzu v adipocytu, inhibuje proteolýzu a zvyšuje syntézu proteinů.
Farmakodynamika
Inzulín detemir je rozpustný, dlouhodobě působící bazální lidský inzulinový analog s relativně plochým akčním profilem. Střední doba působení inzulínu detemiru se pohybovala od 5,7 hodiny při nejnižší dávce do 23,2 hodiny při nejvyšší dávce (doba odběru vzorků 24 hodin).
Prodloužený účinek Levemiru je zprostředkován pomalou systémovou absorpcí inzulínu detemiru molekuly z místa injekce v důsledku silné sebe-asociace molekul léku a albuminu vazba. Inzulín detemir je distribuován pomaleji do periferních cílových tkání, protože inzulin detemir v krevním řečišti je silně vázán na albumin.
Obrázek 1 ukazuje výsledky rychlosti infuze glukózy ze studie glukózové svorky u pacientů s diabetem typu 1.
Obrázek 1: Profily aktivity u pacientů s diabetem typu 1 ve 24hodinové studii s glukózovou svorkou
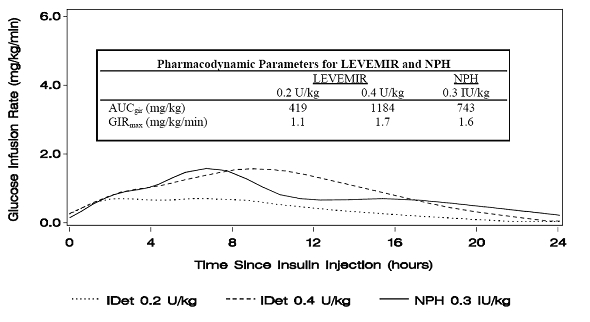
Obrázek 2 ukazuje výsledky rychlosti infuze glukózy ze 16 hodinové studie glukózové svorky u pacientů s diabetem typu 2. Studie svorek byla ukončena 16 hodin podle protokolu.
Obrázek 2: Profily aktivity u pacientů s diabetem typu 2 v 16hodinové studii glukózové svorky

U dávek v intervalu 0,2 až 0,4 U / kg vykazuje Levemir více než 50% svého maximálního účinku od 3 do 4 hodin do přibližně 14 hodin po podání dávky.
Ve studii glukózové svorky celkový glukodynamický účinek (AUCGIR 0-24h) [průměrná mg / kg ± SD (CV)] čtyř samostatných subkutánní injekce do stehna byla 1702,6 ± 489 mg / kg (29%) ve skupině Levemir a 1922,8 ± 765 mg / kg (40%) pro NPH. Klinický význam tohoto rozdílu nebyl stanoven.
Farmakokinetika
Vstřebávání
Po subkutánní injekci inzulínu detemiru u zdravých jedinců a pacientů s diabetem inzulín detemir sérové koncentrace naznačovaly pomalejší, delší prodloužení absorpce během 24 hodin ve srovnání s lidským NPH inzulín.
Maximální koncentrace v séru (Cmax) je dosažena mezi 6 a 8 hodinami po podání.
Absolutní biologická dostupnost inzulínu detemiru je přibližně 60%.
Distribuce a eliminace
Více než 98% inzulínu detemir v krevním řečišti je vázáno na albumin. Levemir má malý zdánlivý distribuční objem přibližně 0,1 l / kg. Levemir má po subkutánním podání terminální poločas 5 až 7 hodin v závislosti na dávce.
Zvláštní populace
Děti a dospívající - Farmakokinetické vlastnosti přípravku Levemir byly zkoumány u dětí (6 až 12 let) a adolescentů (13 až 17 let) a dospělých s diabetem 1. typu. Podobně jako u lidského inzulínu NPH byly pozorovány mírně vyšší plazmatické plochy pod křivkou (AUC) a Cmax u dětí o 10%, respektive o 24%, ve srovnání s dospívajícími a dospělými. Mezi mladistvými a dospělými nebyl žádný rozdíl ve farmakokinetice.
Geriatrie - V klinické studii zkoumající rozdíly ve farmakokinetice jedné subkutánní dávky Levemiru u mladých (25 až 35) let) ve srovnání se staršími zdravými subjekty (â ‰ ¥ 68 let) byly u starších jedinců zjištěny vyšší hladiny AUC inzulínu (až 35%) kvůli sníženému obsahu odbavení. Stejně jako u jiných inzulínových přípravků by měl být Levemir vždy titrován podle individuálních požadavků.
Pohlaví - V kontrolovaných klinických studiích není ve farmakokinetických parametrech na základě analýz podskupin pozorován žádný klinicky relevantní rozdíl mezi pohlavími.
Rasa - Ve dvou studiích se zdravými japonskými a bělošskými jedinci nebyly pozorovány žádné klinicky relevantní rozdíly ve farmakokinetických parametrech. Farmakokinetika a farmakodynamika přípravku Levemir byla zkoumána ve svorkové studii srovnávající pacienty s diabetem 2. typu kavkazského, africko-amerického a latino. Vztahy dávka-odpověď byly srovnatelné pro Levemir v těchto třech populacích.
Poškození ledvin - Jedinci s poškozením ledvin nevykazovali žádný rozdíl ve farmakokinetických parametrech ve srovnání se zdravými dobrovolníky. Zprávy z literatury však ukázaly, že u pacientů s poškozením ledvin je clearance lidského inzulinu snížena. U pacientů s renální dysfunkcí může být nezbytné pečlivé sledování hladiny glukózy a úprava dávky inzulínu, včetně Levemiru (viz OPATŘENÍ, Renální postižení).
Poškození jater - U jedinců s těžkou jaterní dysfunkcí bez diabetu bylo pozorováno, že mají nižší AUC ve srovnání se zdravými dobrovolníky. U pacientů s jaterní dysfunkcí může být nezbytné pečlivé monitorování glukózy a úprava dávky inzulínu, včetně přípravku Levemir OPATŘENÍ, Hepatální poškození).
Těhotenství - Účinek těhotenství na farmakokinetiku a farmakodynamiku přípravku Levemir nebyl studován (viz OPATŘENÍ, Těhotenství).
Kouření - Účinek kouření na farmakokinetiku a farmakodynamiku přípravku Levemir nebyl studován.
horní
Klinické studie
Účinnost a bezpečnost přípravku Levemir podávaného jednou denně před spaním nebo dvakrát denně (před snídaní a před spaním, před snídaní as večerním jídlem nebo ve 12hodinových intervalech) byla srovnávána s studie lidského inzulínu NPH jednou denně nebo dvakrát denně nebo inzulínu glargin jednou denně v neoslepených randomizovaných paralelních studiích s 6004 pacienty s diabetem (3724 s typem 1 a 2280 s typem 2). Obecně dosáhli pacienti léčeni Levemirem hladiny glykemické kontroly podobné těm, kteří byli léčeni lidským inzulínem NPH nebo inzulinem glarginem, měřeno glykosylovaným hemoglobinem (HbA1c).
Diabetes 1. typu - pro dospělé
V jedné nezaslepené klinické studii (studie A, n = 409) byli dospělí pacienti s diabetem 1. typu randomizováni léčba Levemirem ve 12hodinových intervalech, Levemir ráno a před spaním nebo lidský inzulín NPH ráno a před spaním. Inzulín aspart byl také podáván před každým jídlem. Po 16 týdnech léčby měli kombinovaní pacienti léčeni Levemirem podobná snížení HbA1c a plazmatické glukózy nalačno (FPG) jako pacienti léčeni NPH (tabulka 1). Rozdíly v načasování podávání Levemiru (nebo flexibilní dávkování) neměly žádný účinek na HbA1c, FPG, tělesnou hmotnost nebo riziko hypoglykemických epizod.
Celková glykemická kontrola dosažená u přípravku Levemir byla srovnávána s kontrolou dosaženou u inzulínu glargin v randomizované, neslepé klinické studii (Studie B, n = 320), u kterých byli pacienti s diabetem 1. typu léčeni po dobu 26 týdnů buď dvakrát denně (ráno a před spaním) Levemirem, nebo jednou denně (před spaním) inzulínem glargine. Inzulín aspart byl podáván před každým jídlem. U pacientů léčených přípravkem Levemir došlo ke snížení HbA1c podobně jako u pacientů léčených inzulinem glargin.
V randomizované, kontrolované klinické studii (studie C, n = 749) byli pacienti s diabetem 1. typu léčeni jednou denně (před spaním) Levemir nebo lidský inzulín NPH, oba v kombinaci s lidským rozpustným inzulínem před každým jídlem po dobu 6 měsíců. Levemir a lidský inzulín NPH měly podobný účinek na HbA1c.
Tabulka 1: Účinnost a dávkování inzulínu u diabetes mellitus 1. typu - dospělý
| Studie A | ||
| Délka léčby | 16 týdnů | |
| Léčba v kombinaci s | NovoLog® (inzulín aspart) | |
| Levemir | NPH | |
| Počet léčených subjektů | 276 | 133 |
| HbA1c (%) | ||
| Základní hodnota | 8.64 | 8.51 |
| Průměr upravený na konci studie | 7.76 | 7.94 |
| Průměrná změna oproti základní linii | -0.82 | -0.60 |
| Plazmatická glukóza nalačno (mg / dl) | ||
| Průměr upravený na konci studie | 168 | 202 |
| Průměrná změna oproti základní linii | -42.48 | -10.80 |
| Denní bazální dávka inzulínu (U / kg) | ||
| Prestudy znamená | 0.36 | 0.39 |
| Konec studie znamená | 0.49 | 0.45 |
| Denní dávka bolusového inzulínu (U / kg) | ||
| Prestudy znamená | 0.40 | 0.40 |
| Konec studie znamená | 0.38 | 0.38 |
Výchozí hodnoty byly zahrnuty jako kovariáty do analýzy ANCOVA. |
Diabetes 1. typu - dětský
V nezaslepené, randomizované, kontrolované klinické studii (studie D, n = 347) byli pediatričtí pacienti (věkové rozmezí 6 až 17) s diabetem typu 1 léčeni po dobu 26 týdnů bazálním bolusovým inzulinovým režimem. Levemir a lidský inzulín NPH byly podávány jednou nebo dvakrát denně (před spaním nebo ráno a před spaním) podle režimu pretriální dávky. Bolus inzulín aspart byl podáván před každým jídlem. U pacientů léčených Levemirem došlo ke snížení HbA1c podobně jako u lidského inzulinu NPH.
Tabulka 2: Účinnost a dávkování inzulínu u diabetes mellitus 1. typu - dětský
| Studie D | ||
| Délka léčby | 26 týdnů | |
| Léčba v kombinaci s | NovoLog® (inzulín aspart) | |
| Levemir | NPH | |
| Počet léčených subjektů | 232 | 115 |
| HbA1c (%) | ||
| Základní hodnota | 8.75 | 8.77 |
| Průměr upravený na konci studie | 8.02 | 7.93 |
| Průměrná změna oproti základní linii | -0.72 | -0.80 |
| Plazmatická glukóza nalačno (mg / dl) | ||
| Průměr upravený na konci studie | 151.92 | 172.44 |
| Průměrná změna oproti základní linii | -45.00 | -19.98 |
| Denní bazální dávka inzulínu (U / kg) | ||
| Prestudy znamená | 0.48 | 0.49 |
| Konec studie znamená | 0.67 | 0.64 |
| Denní dávka bolusového inzulínu (U / kg) | ||
| Prestudy znamená | 0.52 | 0.47 |
| Konec studie znamená | 0.52 | 0.51 |
Diabetes 2. typu - pro dospělé
Ve 24-týdenní, neoslepené, randomizované klinické studii (studie E, n = 476) byl přípravek Levemir podávaný dvakrát denně (před snídaní a večer) srovnáván s podobným režimem NPH. lidský inzulín jako součást režimu kombinované terapie s jedním nebo dvěma z následujících perorálních antidiabetik (metformin, inzulin sekretagog nebo Î ± glukosidáza) inhibitor). Levemir a NPH podobně snížily HbA1c od základní hodnoty (tabulka 3).
Tabulka 3: Účinnost a dávkování inzulínu u diabetes mellitus 2. typu
| Studie E | ||
| Délka léčby | 24 týdnů | |
| Léčba v kombinaci s | OAD | |
| Levemir | NPH | |
| Počet léčených subjektů | 237 | 239 |
| HbA1c (%) | ||
| Základní hodnota | 8.61 | 8.51 |
| Průměr upravený na konci studie | 6.58 | 6.46 |
| Průměrná změna oproti základní linii | -1.84 | -1.90 |
| Poměr dosahující HbA1c ≤ 7% | 70% | 74% |
| Plazmatická glukóza nalačno (mg / dl) | ||
| Průměr upravený na konci studie | 119.16 | 113.40 |
| Průměrná změna oproti základní linii | -75.96 | -74.34 |
| Denní dávka inzulínu (U / kg) | ||
| Konec studie znamená | 0.77 | 0.52 |
V 22týdenní, neoslepené, randomizované klinické studii (studie F, n = 395) u dospělých s diabetem 2. typu byl Levemir a lidský inzulín NPH podáván jednou nebo dvakrát denně v rámci režimu bazálního bolusu. Jak bylo měřeno pomocí HbA1c nebo FPG, měl Levemir účinnost podobnou lidskému inzulinu NPH.
horní
Indikace a použití
Levemir je indikován k subkutánnímu podání jednou nebo dvakrát denně k léčbě dospělých a pediatrických pacientů s typem 1 diabetes mellitus nebo dospělí pacienti s diabetes mellitus 2. typu, kteří vyžadují bazální (dlouhodobě působící) inzulín pro kontrolu hyperglykémie.
horní
Kontraindikace
Levemir je kontraindikován u pacientů s přecitlivělostí na inzulin detemir nebo na některou z pomocných látek.
horní
Varování
Hypoglykémie je nejčastějším nepříznivým účinkem inzulínové terapie, včetně Levemiru. Stejně jako u všech inzulínů se načasování hypoglykémie může u různých inzulínových přípravků lišit.
Monitorování glukózy se doporučuje všem pacientům s diabetem.
Levemir se nesmí používat v inzulínových infuzních pumpách.
Jakákoli změna dávky inzulínu by měla být prováděna opatrně a pouze pod lékařským dohledem. Změny síly inzulínu, načasování dávkování, výrobce, typ (např. Normální, NPH nebo analogy inzulínu), druh (zvíře, člověk) nebo způsob výroby (rDNA versus zvíře-zdroj inzulínu) může vést k potřebě změny v dávkování.
Může být nutné upravit souběžnou perorální antidiabetickou léčbu.
horní
Opatření
Všeobecné
Nedostatečné dávkování nebo přerušení léčby může vést k hyperglykémii au pacientů s diabetem 1. typu k diabetické ketoacidóze. První příznaky hyperglykémie se obvykle objevují postupně v průběhu hodin nebo dnů. Patří mezi ně nevolnost, zvracení, ospalost, zčervenaná suchá kůže, sucho v ústech, zvýšené močení, žízeň a ztráta chuti k jídlu, stejně jako acetonový dech. Neléčené hyperglykemické příhody jsou potenciálně fatální.
Levemir není určen pro intravenózní ani intramuskulární podání. Prodloužené trvání aktivity inzulínu detemiru závisí na injekci do podkožní tkáně. Intravenózní podání obvyklé subkutánní dávky může vést k těžké hypoglykémii. Absorpce po intramuskulárním podání je rychlejší a rozsáhlejší než absorpce po subkutánním podání.
Levemir by neměl být naředěn nebo smíchán s jinými inzulínovými přípravky (viz OPATŘENÍ, Míchání inzulínů).
Inzulín může způsobit retenci sodíku a otoky, zejména pokud se dříve zeslabená metabolická kontrola zlepší intenzivní inzulinovou terapií.
Lipodystrofie a přecitlivělost patří mezi potenciální klinické nežádoucí účinky spojené s užíváním všech inzulínů.
Stejně jako u všech inzulínových přípravků se časový průběh účinku Levemiru může lišit u různých jedinců nebo v různé časy u stejného jedince a závisí na místě injekce, krevním zásobení, teplotě a fyzickém stavu aktivita.
Úprava dávky jakéhokoli inzulínu může být nezbytná, pokud pacienti změní svou fyzickou aktivitu nebo svůj obvyklý jídelní plán.
Hypoglykémie
Stejně jako u všech inzulínových přípravků může být s podáváním přípravku Levemir spojena hypoglykemická reakce. Hypoglykémie je nejčastějším nepříznivým účinkem inzulínů. Včasné varovné příznaky hypoglykémie se mohou za určitých podmínek, například dlouhé, lišit trvání diabetu, onemocnění diabetického nervu, použití léků, jako jsou beta-blokátory, nebo zesílená kontrola diabetu (vidět OPATŘENÍ, Lékové interakce). Takové situace mohou vést k těžké hypoglykémii (a možná ke ztrátě vědomí) před tím, než si pacient uvědomí hypoglykémii.
Čas výskytu hypoglykémie závisí na profilu účinku použitých inzulínů, a proto se může změnit, když se změní léčebný režim nebo načasování dávkování. U pacientů, kteří přecházejí z jiných střednědobých nebo dlouhodobě působících inzulínových přípravků na Levemir jednou nebo dvakrát denně, mohou být dávky předepsány na jednotkové bázi; ale stejně jako u všech inzulínových přípravků může být nutné upravit dávku a načasování podávání, aby se snížilo riziko hypoglykémie (viz DÁVKOVÁNÍ A PODÁNÍ, Přechod na Levemir).
Renální postižení
Stejně jako u jiných inzulínů může být nutné upravit požadavky na Levemir u pacientů s poškozením ledvin (viz KLINICKÁ FARMAKOLOGIE, Farmakokinetika).
Jaterní postižení
Stejně jako u jiných inzulínů může být nutné upravit požadavky na Levemir u pacientů se zhoršenou funkcí jater (viz KLINICKÁ FARMAKOLOGIE, Farmakokinetika).
Místo vpichu a alergické reakce
Stejně jako u každé inzulínové terapie se v místě vpichu může objevit lipodistrofie a oddálit absorpci inzulínu. Jiné reakce v místě vpichu s inzulinovou terapií mohou zahrnovat zarudnutí, bolest, svědění, kopřivku, otok a zánět. Neustálé střídání místa vpichu v dané oblasti může pomoci zmírnit nebo zabránit těmto reakcím. Reakce obvykle ustoupí během několika dnů až několika týdnů. Ve vzácných případech mohou reakce v místě vpichu vyžadovat ukončení léčby Levemirem.
V některých případech mohou tyto reakce souviset s jinými faktory než inzulinem, jako jsou dráždivé látky v přípravku na čištění kůže nebo špatná technika injekce.
Systémová alergie: Generalizovaná alergie na inzulín, která je méně častá, ale potenciálně závažnější, může způsobit vyrážku (včetně svědění) na celém těle, dušnost, sípání, snížení krevního tlaku, rychlý puls nebo pocení. Závažné případy generalizované alergie, včetně anafylaktické reakce, mohou být život ohrožující.
Interkurentní podmínky
Požadavky na inzulín mohou být změněny během interkurentních stavů, jako jsou nemoci, emoční poruchy nebo jiné stresy.
Informace pro pacienty
Levemir se smí použít pouze tehdy, je-li roztok čirý a bezbarvý bez viditelných částic (viz DÁVKOVÁNÍ A PODÁNÍ, Příprava a manipulace). Pacienti by měli být informováni o možných rizicích a výhodách léčby Levemirem, včetně možných vedlejších účinků. Pacientům by mělo být nabídnuto další vzdělávání a poradenství v oblasti inzulínových terapií, injekční techniky, životního stylu, pravidelného monitorování glukózy, periodického testování glykosylovaného hemoglobinu, rozpoznání a řízení hypo- a hyperglykémie, dodržování plánování jídla, komplikace inzulínové terapie, načasování dávkování, návod na použití injekčních zařízení a správné skladování inzulín. Pacienti by měli být informováni o tom, že k dosažení účinné kontroly glykémie jsou nutná častá měření glykémie prováděná pacientem, aby se zabránilo hyperglykémii i hypoglykémii. Pacienti musí být poučeni o řešení zvláštních situací, jako jsou interkurentní stavy (nemoc, stres nebo emoční) poruchy), nepřiměřená nebo přeskočená dávka inzulínu, neúmyslné podání zvýšené dávky inzulínu, nedostatečný příjem potravy nebo vynechaná jídla. Další informace naleznete v kolonce „Informace pro pacienty“ Levemiru.
Stejně jako u všech pacientů s cukrovkou může být schopnost koncentrace a / nebo reakce snížena v důsledku hypoglykémie nebo hyperglykémie.
Pacientky s diabetem by měly být informovány, aby informovaly svého zdravotnického pracovníka, pokud jsou těhotné nebo uvažují o těhotenství (viz OPATŘENÍ, Těhotenství).
Laboratorní testy
Stejně jako u každé inzulínové terapie by měla být terapeutická odpověď na Levemir sledována periodickými testy na krevní glukózu. Pro monitorování dlouhodobé kontroly glykémie se doporučuje pravidelné měření HbA1c.
Lékové interakce
Řada látek ovlivňuje metabolismus glukózy a může vyžadovat úpravu dávky inzulínu a zvláště pečlivé sledování.
Níže jsou uvedeny příklady látek, které mohou snižovat účinek inzulínu na snižování hladiny glukózy v krvi: kortikosteroidy, danazol, diuretika, sympatomimetika (např. epinefrin, albuterol, terbutalin), isoniazid, deriváty fenothiazinu, somatropin, hormony štítné žlázy, estrogeny, progestogeny (např. orálně antikoncepční prostředky).
Následuje příklad látek, které mohou zvýšit účinek inzulínu na snížení hladiny glukózy v krvi a náchylnost k hypoglykémii: orální antidiabetika léky, ACE inhibitory, disopyramid, fibráty, fluoxetin, MAO inhibitory, propoxyfen, salicyláty, analog somatostatinu (např. oktreotid) a sulfonamid antibiotika.
Beta-blokátory, klonidin, lithné soli a alkohol mohou buď zesílit nebo oslabit účinek inzulínu na snížení hladiny glukózy v krvi. Pentamidin může způsobit hypoglykémii, po které může někdy následovat hyperglykémie. Kromě toho mohou být pod vlivem sympatolytických léčivých přípravků, jako jsou beta-blokátory, klonidin, guanethidin a reserpin, sníženy nebo chybějící příznaky hypoglykémie.
Výsledky studií vazby na proteiny in vitro a in vivo ukazují, že neexistuje žádná klinicky relevantní interakce mezi inzulinem detemir a mastnými kyselinami nebo jinými léky vázanými na proteiny.
Míchání inzulínů
Pokud je Levemir smíchán s jinými inzulínovými přípravky, může se změnit profil účinku jedné nebo obou jednotlivých složek. Míchání přípravku Levemir s inzulínem aspartem, rychle působícím analogem inzulínu, vedlo k přibližně 40% snížení AUC (0-2h) a Cmax pro inzulín aspart ve srovnání se samostatnými injekcemi, když byl poměr inzulinu aspart k Levemiru nižší než 50%.
Levemir NESMÍ být míchán nebo ředěn s jinými inzulínovými přípravky.
Karcinogeneze, mutageneze, zhoršení plodnosti
Standardní dvouleté studie karcinogenity u zvířat nebyly provedeny. Inzulin detemir testoval negativní na genotoxický potenciál v in vitro studii reverzní mutace in vitro bakterií, testu aberace chromozomových aberací lymfocytů lidské periferní krve a myši in vivo mikronukleární test.
Těhotenství
Kategorie těhotenství C
Teratogenní účinky
Ve studii plodnosti a embryonálního vývoje byl inzulin detemir podáván samicím potkanů před pářením, během páření a během těhotenství v dávkách až 300 nmol / kg / den (3krát větší než doporučená dávka pro člověka, na základě plazmatické plochy pod křivkou (AUC)) poměr). Dávky 150 a 300 nmol / kg / den vyvolaly počty vrhů s viscerálními anomáliemi. Během organogeneze byly králíkům podávány dávky až do 900 nmol / kg / den (přibližně 135násobek doporučené dávky pro člověka na základě poměru AUC). Při dávce 900 nmol / kg / den bylo pozorováno zvýšení incidence plodů s abnormalitami žlučníku související s dávkou léčiva, jako jsou malé, bilobované, rozdvojené a chybějící žlučníky. Studie embryofetálního vývoje potkanů a králíků, které obsahovaly souběžné kontrolní skupiny pro lidský inzulín uvedl, že inzulin detemir a lidský inzulín mají podobné účinky, pokud jde o embryotoxicitu a teratogenita.
Kojící matky
Není známo, zda se Levemir vylučuje ve významném množství do mateřského mléka. Z tohoto důvodu je třeba při podávání Levemiru kojící matce postupovat opatrně. Pacienti s diabetem, kteří kojí, mohou vyžadovat úpravu dávky inzulínu, stravovacího plánu nebo obojí.
Pediatrické použití
V kontrolované klinické studii byly koncentrace HbA1c a míry hypoglykémie podobné u pacientů léčených přípravkem Levemir a pacientů léčených lidským inzulínem NPH.
Geriatrické použití
Z celkového počtu subjektů v přechodných a dlouhodobých klinických studiích s Levemirem bylo 85 (studie typu 1) a 363 (studie typu 2) 65 let a více. Mezi těmito jedinci a mladšími osobami nebyly pozorovány žádné celkové rozdíly v bezpečnosti nebo účinnosti a jiné hlášené klinické zkušenosti mají nebyly identifikovány rozdíly v odpovědích mezi staršími a mladšími pacienty, ale nelze vyloučit větší citlivost některých starších jedinců. U starších pacientů s diabetem by mělo být počáteční dávkování, zvyšování dávky a udržovací dávka konzervativní, aby se zabránilo hypoglykemickým reakcím. U starších pacientů může být obtížné rozpoznat hypoglykémii.
horní
Nežádoucí reakce
Mezi nežádoucí příhody obvykle spojené s léčbou lidským inzulínem patří:
Tělo jako celek: alergické reakce (viz OPATŘENÍ, Alergie).
Kůže a dodatky: lipodystrofie, svědění, vyrážka. Mírné reakce v místě vpichu se vyskytly častěji s Levemirem než s lidským inzulínem NPH a obvykle ustoupily během několika dnů až několika týdnů (viz OPATŘENÍ, Alergie).
Jiný:
Hypoglykémie: (viz VAROVÁNÍ a OPATŘENÍ).
Ve studiích trvajících až 6 měsíců u pacientů s diabetem 1. a 2. typu byl výskyt těžké hypoglykémie s Levemir byl srovnatelný s incidencí s NPH a podle očekávání byl celkově vyšší u pacientů s diabetem 1. typu (tabulka 1) 4).
Přibývání na váze:
Ve studiích trvajících až 6 měsíců u pacientů s diabetem 1. a 2. typu byl Levemir spojen s poněkud menším přírůstkem hmotnosti než NPH (tabulka 4). Není známo, zda tyto pozorované rozdíly představují skutečné rozdíly v účincích Levemiru a NPH inzulínu, protože tyto studie nebyly oslepeny a protokoly (např. pokyny o stravě a cvičení a monitorování) nebyly konkrétně zaměřeny na zkoumání hypotéz souvisejících s hmotnostními účinky léčby v porovnání. Klinický význam pozorovaných rozdílů nebyl stanoven.
Tabulka 4: Bezpečnostní informace o klinických studiích *
| ||||||
| váha (kg) | Hypoglykémie (události / subjekt / měsíc) | |||||
| Léčba | Počet předmětů | Základní hodnota | Konec léčby | Hlavní, důležitý†| Méně důležitýC | |
| Typ 1 | ||||||
| Studie A | Levemir | N = 276 | 75.0 | 75.1 | 0.045 | 2.184 |
| NPH | N = 133 | 75.7 | 76.4 | 0.035 | 3.063 | |
| Studie C | Levemir | N = 492 | 76.5 | 76.3 | 0.029 | 2.397 |
| NPH | N = 257 | 76.1 | 76.5 | 0.027 | 2.564 | |
| Studie D Pediatric | Levemir | N = 232 | N / A | N / A | 0.076 | 2.677 |
| NPH | N = 115 | N / A | N / A | 0.083 | 3.203 | |
| Typ 2 | ||||||
| Studie E | Levemir | N = 237 | 82.7 | 83.7 | 0.001 | 0.306 |
| NPH | N = 239 | 82.4 | 85.2 | 0.006 | 0.595 | |
| Studie F | Levemir | N = 195 | 81.8 | 82.3 | 0.003 | 0.193 |
| NPH | N = 200 | 79.6 | 80.9 | 0.006 | 0.235 |
horní
Předávkování
Hypoglykémie se může objevit v důsledku nadměrného množství inzulínu vzhledem k příjmu potravy, výdaji energie nebo obojí. Mírné epizody hypoglykémie lze obvykle léčit perorální glukózou. Může být nutné upravit dávkování léků, vzorce jídla nebo cvičení. Závažnější epizody s kómou, křečemi nebo neurologickým poškozením mohou být léčeny intramuskulárním / subkutánním glukagonem nebo koncentrovanou intravenózní glukózou. Po zjevném klinickém zotavení z hypoglykémie může být nezbytné další pozorování a další příjem uhlohydrátů, aby nedošlo k opětovnému výskytu hypoglykémie.
horní
Dávkování a správa
Levemir může být podáván jednou nebo dvakrát denně. Dávka Levemiru by měla být upravena podle měření hladiny glukózy v krvi. Dávkování Levemiru by mělo být individualizováno na základě doporučení lékaře v souladu s potřebami pacienta.
- U pacientů léčených Levemirem jednou denně by měla být dávka podávána s večerním jídlem nebo před spaním.
- U pacientů, kteří vyžadují účinnou kontrolu hladiny glukózy v krvi dvakrát denně, může být večerní dávka podána s večerním jídlem, před spaním nebo 12 hodin po ranní dávce.
Levemir by měl být podáván subkutánní injekcí do stehna, břišní stěny nebo paže. Místa vpichu by se měla otáčet ve stejné oblasti. Stejně jako u všech inzulínů se trvání účinku bude lišit v závislosti na dávce, místě vpichu, průtoku krve, teplotě a úrovni fyzické aktivity.
Stanovení dávky pro Levemir
- U pacientů s diabetem 1. nebo 2. typu léčených bazálním bolusem může být bazální inzulín změněn na Levemir na jednotce. Dávka Levemiru by pak měla být upravena tak, aby bylo dosaženo glykemických cílů. U některých pacientů s diabetem 2. typu může být zapotřebí více Levemiru než NPH inzulínu. V klinické studii byla průměrná dávka na konci léčby 0,77 U / kg pro Levemir a 0,52 IU / kg pro lidský inzulín NPH (viz viz Tabulka 3).
- U pacientů, kteří v současné době užívají pouze bazální inzulín, lze změnit bazální inzulín na Levemir na jednotce.
- U pacientů s inzulinem dosud neléčených diabetu 2. typu, kteří jsou nedostatečně kontrolováni perorálními antidiabetiky, by měl být přípravek Levemir zahájen v dávce 0,1 až 0,2 U / kg jednou denně večer nebo 10 jednotek jednou nebo dvakrát denně a dávka se upraví tak, aby se dosáhlo glykémie cíle.
- Stejně jako u všech inzulínů se během přechodu a v prvních týdnech po něm doporučuje pečlivé monitorování glukózy. Může být nutné upravit dávku a načasování současných krátkodobě působících inzulínů nebo jinou současnou antidiabetickou léčbu.
Příprava a manipulace
Levemir by měl být před podáním vizuálně zkontrolován a měl by být použit pouze tehdy, je-li roztok čirý a bezbarvý.
Levemir by neměl být mísen nebo ředěn s jinými inzulínovými přípravky.
Po každé injekci musí pacient odstranit jehlu bez opětovného uzavření a zlikvidovat ji v nádobě odolné proti propíchnutí. Použité injekční stříkačky, jehly nebo lancety by měly být umístěny do „ostrých“ nádob (například do červeného biohazardu) kontejnery), tvrdé plastové kontejnery (jako jsou lahve na čisticí prostředky) nebo kovové kontejnery (například prázdné) káva může). Tyto nádoby by měly být utěsněny a řádně zlikvidovány.
horní
Jak dodáván
Levemir je k dispozici v následujících velikostech balení: každá prezentace obsahuje 100 jednotek inzulínu detemiru na ml (U-100).
| 10 ml lahvička | NDC 0169-3687-12 |
| 3 ml PenFill® kazety * | NDC 0169-3305-11 |
| 3 ml InnoLet® | NDC 0169-2312-11 |
| 3 ml FlexPen® | NDC 0169-6439-10 |
* Zásobníky Levemir PenFill® jsou určeny k použití s aplikacemi Novo Nordisk 3 mL PenFill® kompatibilními s inzertem a jednorázovými jehlami NovoFine®.
Poslední aktualizace 05/2007
Levemir, inzulin detemir (původ rDNA), informace o pacientech (v prosté angličtině)
Podrobné informace o příznacích, příznacích, příčinách, léčbě cukrovky
Účelem informací v této monografii není pokrýt všechna možná použití, pokyny, preventivní opatření, lékové interakce nebo nepříznivé účinky. Tyto informace jsou zobecněné a neslouží jako zvláštní lékařská pomoc. Máte-li dotazy týkající se léků, které užíváte, nebo byste chtěli získat více informací, obraťte se na svého lékaře, lékárníka nebo zdravotní sestru.
zpět k: Procházet všechny léky na cukrovku



