Symlin pro léčbu cukrovky
Název značky: Symlin, Symlin Pen
Obecný název: pramlintid acetát
Obsah:
Popis
Farmakologie
Klinické studie
Indikace a použití
Kontraindikace
Varování
Opatření
Nežádoucí reakce
Předávkovat
Dávkování a správa
Jak dodáván
Úložný prostor
Symlin, Symlin Pen, pramlintide acetát, informace o pacientech
VAROVÁNÍ
Přípravek Symlin se používá s inzulínem a byl spojen se zvýšeným rizikem těžké hypoglykémie vyvolané inzulínem, zejména u pacientů s diabetem 1. typu. Pokud dojde k závažné hypoglykémii spojené s užíváním Symlinu, je to vidět do 3 hodin po injekci Symlin. Dojde-li k závažné hypoglykémii při provozu motorového vozidla, těžkých strojů nebo při provádění jiných vysoce rizikových činností, může dojít k vážným zraněním. Vhodným výběrem pacienta, pečlivým poučením pacienta a úpravou dávky inzulínu jsou kritické prvky pro snížení tohoto rizika.
Popis
Injekce Symlin® (pramlintid acetát) je antihyperglykemické léčivo pro použití u pacientů s diabetem léčených inzulinem. Pramlintid je syntetický analog lidského amylinu, přirozeně se vyskytujícího neuroendokrinního hormonu syntetizovaného pankreatickými beta buňkami, který přispívá ke kontrole glukózy během postprandiálního období. Pramlintid je poskytován jako acetátová sůl syntetického polypeptidu s 37 aminokyselinami, který se liší v amino kyselinová sekvence z lidského amylinu nahrazením prolinem v pozicích 25 (alanin), 28 (serin) a 29 (serine).
Strukturální vzorec acetátu pramlintidu je znázorněn:

Pramlintidacetát je bílý prášek, který má molekulový vzorec C171H267N51O53S2- x C2H4O2 (3â ‰ ¤xâ ‰ ¤8); molekulová hmotnost je 3949,4. Pramlintid acetát je rozpustný ve vodě.
Symlin je formulován jako čirý, izotonický sterilní roztok pro subkutánní (SC) podání. Jednorázová injekční stříkačka SymlinPen® pro více dávek obsahuje 1 000 mcg / ml pramlintidu (jako acetát); Injekční lahvičky Symlin obsahují 600 mcg / ml pramlintidu (jako acetát). Obě formulace obsahují 2,25 mg / ml metakresolu jako konzervačního činidla, D-mannitol jako modifikátor tonicity a kyselinu octovou a octan sodný jako modifikátory pH. Symlin má pH přibližně 4,0.
horní
Klinická farmakologie
Amylinova fyziologie
Amylin je společně lokalizován s inzulínem v sekrečních granulích a ko-sekretován s inzulinem pankreatickými beta buňkami v reakci na příjem potravy. Amylin a inzulín vykazují podobné postní a postprandiální vzorce u zdravých jedinců (obrázek 1).
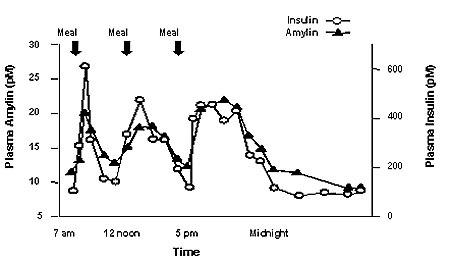
Obrázek 1: Profil sekrece amylínu a inzulínu u zdravých dospělých
Amylin ovlivňuje rychlost postprandiální glukózy prostřednictvím různých mechanismů. Amylin zpomaluje vyprazdňování žaludku (tj. Rychlost uvolňování potravy ze žaludku do tenkého střeva), aniž by došlo ke změně celkové absorpce živin. Kromě toho amylin potlačuje sekreci glukagonu (není normalizován samotným inzulínem), což vede k potlačení endogenní produkce glukózy z jater. Amylin také reguluje příjem potravy díky centrálně zprostředkované modulaci chuti k jídlu.
U pacientů s diabetem typu 2 nebo 1 používajícím inzulin jsou pankreatické beta buňky nefunkční nebo poškozené, což má za následek sníženou sekreci inzulínu a amylinu v reakci na jídlo.
Mechanismus účinku
Symlin působí jako amylinomimetikum a má následující účinky: 1) modulace vyprazdňování žaludku; 2) prevence postprandiálního vzestupu plazmatického glukagonu; a 3) sytost vedoucí ke sníženému příjmu kalorií a možnému úbytku hmotnosti.
Vyprazdňování žaludku
Rychlost vyprazdňování žaludku je důležitým určujícím faktorem postprandiálního vzestupu plazmatické glukózy. Symlin zpomaluje rychlost uvolňování potravy ze žaludku do tenkého střeva po jídle, a tak snižuje počáteční postprandiální zvýšení hladiny glukózy v plazmě. Tento účinek trvá přibližně 3 hodiny po podání Symlin. Symlin nemění čistou absorpci přijímaného uhlohydrátu nebo jiných živin.
Postprandiální sekrece glukagonu
U pacientů s diabetem jsou koncentrace glukagonu během postprandiálního období abnormálně zvýšené, což přispívá k hyperglykémii. Bylo prokázáno, že Symlin snižuje postprandiální koncentrace glukagonu u pacientů s diabetem užívajících inzulín.
Sytost
Ukázalo se, že Symlin podávaný před jídlem snižuje celkový kalorický příjem. Zdá se, že tento účinek je nezávislý na nevolnosti, která může doprovázet léčbu Symlinem.
Farmakokinetika
Vstřebávání
Absolutní biologická dostupnost jediné SC dávky Symlin je přibližně 30 až 40%. Subkutánní podání různých dávek Symlinu do břišní oblasti nebo stehna zdravých jedinců vedlo k maximální plazmatické koncentraci úměrné dávce (Cmax) a celková expozice (vyjádřená jako plocha pod křivkou plazmatické koncentrace nebo (AUC)) (tabulka 1).
Tabulka 1: Průměrné farmakokinetické parametry po podání jediné dávky Symlinu SC
| SC Dose (mcg) |
AUC (0-β) (pmol * min / L) |
Cmax (pmol / l) |
Tmax (min) |
Eliminace t ½ (min) |
|---|---|---|---|---|
| 30 | 3750 | 39 | 21 | 55 |
| 60 | 6778 | 79 | 20 | 49 |
| 90 | 8507 | 102 | 19 | 51 |
| 120 | 11970 | 147 | 21 | 48 |
Injekce Symlin do paže vykazovala vyšší expozici s větší variabilitou ve srovnání s expozicí po injekci Symlin do břišní oblasti nebo stehna.
Nebyla zjištěna žádná silná korelace mezi stupněm adipozity, jak bylo stanoveno pomocí měření BMI nebo tloušťky kožních záhybů, a relativní biologickou dostupností. Injekce podávané s jehlami 6,0 mm a 12,7 mm poskytly podobnou biologickou dostupnost.
Rozdělení
Symlin se příliš neváže na krvinky ani na albumin (přibližně 40% léčiva je nevázáno v plazmě), a proto by měla být jeho farmakokinetika necitlivá na změny vazebných míst.
Metabolismus a eliminace
U zdravých jedinců je poločas Symlinu přibližně 48 minut. Symlin je metabolizován především ledvinami. Des-lys1 pramlintid (2-37 pramlintid), primární metabolit, má podobný poločas a biologicky aktivní u potkanů in vitro i in vivo. Hodnoty AUC jsou při opakovaném dávkování relativně konstantní, což znamená, že nedochází k bioakumulaci.
Zvláštní populace
Renální nedostatečnost
Pacienti se středně těžkou nebo těžkou poruchou funkce ledvin (ClCr> 20 až ± 50 ml / min) nevykazovali zvýšenou expozici Symlin nebo sníženou clearance Symlin ve srovnání s jedinci s normální funkcí ledvin. U dialyzovaných pacientů nebyly provedeny žádné studie.
Jaterní nedostatečnost
Farmakokinetické studie u pacientů s jaterní nedostatečností nebyly provedeny. Na základě velkého stupně renálního metabolismu (viz Metabolismus a vylučování) se však neočekává, že by jaterní dysfunkce ovlivňovala koncentraci Symlin v krvi.
Geriatrické
Farmakokinetické studie u geriatrické populace nebyly provedeny. Přípravek Symlin by měl být používán pouze u pacientů, o nichž je známo, že plně rozumí a dodržují správné úpravy inzulínu a monitorování glukózy. V geriatrické populaci nebyly pozorovány konzistentní věkové rozdíly v aktivitě Symlinu (n = 539 u pacientů ve věku 65 let a starších v klinických studiích).
Pediatric
Symlin nebyl v pediatrické populaci hodnocen.
Rod
Nebyla provedena žádná studie, která by vyhodnotila možné genderové účinky na farmakokinetiku Symlin. V klinických studiích však nebyly pozorovány žádné konzistentní genderové rozdíly v aktivitě Symlin (n = 2799 pro muže a n = 2085 pro ženy).
Rasa / etnicita
Nebyla provedena žádná studie hodnotící účinek etnicity na farmakokinetiku Symlin. U pacientů s odlišnými pacienty však nebyly pozorovány žádné konzistentní rozdíly v aktivitě Symlinu rasa / etnicita v klinických studiích (n = 4257 pro bílou, n = 229 pro černou, n = 337 pro hispánskou a n = 61 pro ostatní) etnický původ).
Lékové interakce
Účinek přípravku Symlin (120 mcg) na farmakokinetiku acetaminofenu (1000 mg) jako markeru vyprazdňování žaludku byl hodnocen u pacientů s diabetem 2. typu (n = 24). Symlin významně nezměnil AUC acetaminofenu. Symlin však snížil acetaminofen Cmax (asi 29% při současném současném podávání) a prodloužil čas na maximální plazmatickou koncentraci nebo tmax (v rozmezí 48 až 72 minut) v závislosti na době podání acetaminofenu vzhledem k injekci Symlin. Symlin významně neovlivnil acetaminofen tmax když byl acetaminofen podán 1 až 2 hodiny před injekcí Symlin. Nicméně, tmax acetaminofenu byl významně zvýšen, když byl acetaminofen podáván současně s injekcí Symlin nebo do 2 hodin po injekci Symlin (viz OPATŘENÍ, Lékové interakce).
Farmakodynamika
V klinických studiích u pacientů s diabetem typu 2 a 1 používajícím inzulín došlo k podávání přípravku Symlin ve snížení průměrných postprandiálních koncentrací glukózy, snížení fluktuací glukózy a snížení potravy příjem. Dávky Symlinu se liší u pacientů užívajících inzulín typu 2 a typu 1 (viz DÁVKOVÁNÍ A PODÁNÍ).
Snížení postprandiálních koncentrací glukózy
Symlin podávaný subkutánně bezprostředně před jídlem snížil koncentrace glukózy v plazmě po jídle, když se používal s běžným inzulinem nebo rychle působícími analogy inzulinu (obrázek 2). Toto snížení postprandiální glukózy snížilo množství potřebného krátkodobě působícího inzulínu a omezilo kolísání glukózy na základě 24hodinového monitorování glukózy. Když byly použity rychle působící analogové inzulíny, koncentrace glukózy v plazmě měla tendenci stoupat v intervalu mezi 150 minutami po injekci Symlinu a dalším jídlem (viz DÁVKOVÁNÍ A PODÁNÍ).

Obrázek 2: Profily glukózy v plazmě po jídle u pacientů s diabetem 2. a 1. typu, kteří dostávají Symlin a / nebo inzulín
Snížený příjem potravin
Jedna, subkutánní dávka Symlin 120 mcg (typ 2) nebo 30 mcg (typ 1) podaná 1 hodinu před neomezeným jídlem formou bufetu byla spojena s snížení celkového kalorického příjmu (průměrné změny odečtené od placeba o ~ 23%, respektive 21%), k nimž došlo bez snížení jídla doba trvání.
horní
Klinické studie
V klinických studiích dostalo Symlin celkem 5325 pacientů a zdravých dobrovolníků. To zahrnuje 1688 s diabetem typu 2 a 2375 s diabetem typu 1 u krátkodobě a dlouhodobě kontrolovaných klinických studií, dlouhodobých nekontrolovaných klinických hodnocení a otevřené studie v klinické praxi nastavení.
Klinické studie u diabetu 2. typu
Účinnost rozmezí dávek Symlin byla hodnocena v několika placebem kontrolovaných a otevřených klinických studiích u pacientů užívajících inzulín s diabetem 2. typu. Na základě výsledků získaných v těchto studiích je doporučená dávka přípravku Symlin pro pacienty s cukrovkou typu 2 užívající inzulín 120 mcg podaná bezprostředně před hlavním jídlem.
U pacientů s diabetem typu 2 byly provedeny dvě, dlouhodobé (26 až 52 týdnů) randomizované, dvojitě zaslepené, placebem kontrolované studie s použitím inzulínu s fixní dávkou k izolaci účinku Symlin. Demografické a výchozí charakteristiky u 871 pacientů léčených Symlinem jsou následující: průměrná výchozí hodnota HbA1c se pohybovala od 9,0 do 9,4%, průměrný věk byl 56,4 až 59,1 let, průměrné trvání diabetu se pohybovalo od 11,5 do 14,4 let a průměrné BMI se pohybovalo od 30,1 do 34,4 kg / m2. V obou těchto studiích byl Symlin nebo placebo přidán k existujícím diabetickým terapiím účastníků, které obsahovaly inzulín s nebo bez sulfonylmočovinového činidla a / nebo metforminu.
Tabulka 2 shrnuje složené výsledky v obou studiích u pacientů, kterým byla přidělena dávka 120 mcg po 6 měsících léčby.
Tabulka 2: Průměrná (SE) změna v HbA1c, hmotnosti a inzulínu po 6 měsících ve dvojitě slepých, placebem kontrolovaných studiích u pacientů s inzulínem typu 2
| Proměnná | Placebo | Symlin (120 mcg) |
|---|---|---|
| Výchozí hodnota HbA1c (%) | 9.3 (0.08) | 9.1 (0.06) |
| Změna HbA1c po 6 měsících ve srovnání s výchozím stavem (%) | −0.17 (0.07) | −0.57 (0.06)* |
| Placebem odečtená změna HbA1c po 6 měsících (%) | NA | −0.40 (0.09)* |
| Základní hmotnost (kg) | 91.3 (1.2) | 92.5 (1.2) |
| Změna hmotnosti po 6 měsících ve srovnání s výchozím stavem (kg) | +0.2 (0.2) | −1.5 (0.2)* |
| Změna hmotnosti odečtená podle placeba po 6 měsících (kg) | NA | −1.7 (0.3)* |
| Procentní změna inzulínových dávek po 6 měsících: rychlé / krátkodobé působení | +6.5 (2.7) | −3.0 (1.6)* |
| Procentní změna inzulínových dávek po 6 měsících: dlouhodobě působící | +5.2 (1.4) | −0.2 (1.3)* |
|
V kohortě 145 pacientů, kteří dokončili dva roky léčby Symlinem, byly odečteny HbA1c a snížení hmotnosti o výchozí hodnotu: 0,40% a 0,36 kg.
Otevřená studie v prostředí klinické praxe
Otevřená studie Symlin byla provedena v doporučené dávce 120 mcg u 166 pacientů s diabetem typu 2, kteří nebyli schopni dosáhnout glykemických cílů pomocí samotného inzulínu. U těchto pacientů byl použit režim inzulinu s flexibilní dávkou (viz DÁVKOVÁNÍ A PODÁNÍ). V této studii pacienti upravovali svůj inzulinový režim na základě monitorování glukózy před jídlem a po jídle. Na začátku studie byl průměrný HbA1c 8,3%, průměrný věk byl 54,4 let, průměrné trvání diabetu bylo 13,3 let a průměrný BMI byl 38,6 kg / m2. Symlin byl podáván s hlavním jídlem. Léčba přípravkem Symlin plus inzulínem po dobu 6 měsíců vedla k průměrnému snížení HbA1c odečtenému od základní hodnoty o 0,56 ± 0,15% a průměrnému snížení hmotnosti odečtenému od základu o 2,76 ± 0,34 kg. Tyto změny byly provedeny snížením dávek celkového, krátkodobě působícího a dlouhodobě působícího inzulínu (66,4 ± 2,66, .3 10,3 ± 4,84 a .204,20 ± 2,42%).
Klinické studie u diabetu 1. typu
Účinnost rozmezí dávek Symlin byla hodnocena v několika placebem kontrolovaných a otevřených klinických studiích prováděných u pacientů s diabetem 1. typu. Na základě výsledků získaných v těchto studiích je doporučená dávka přípravku Symlin pro pacienty s diabetem typu 1 30 mcg nebo 60 mcg podaná bezprostředně před hlavním jídlem.
U pacientů s diabetem 1. typu byly provedeny tři, dlouhodobé (26 až 52 týdnů), randomizované, dvojitě slepé, placebem kontrolované studie Symlin (N = 1717). Dvě z těchto studií umožnily pouze minimální úpravy inzulínu, aby se izoloval účinek Symlin; ve třetí studii byly úpravy inzulínu provedeny podle standardní lékařské praxe. Demografické a výchozí charakteristiky u 1179 pacientů léčených Symlinem byly následující: průměrné výchozí rozmezí HbA1c bylo 8,7 až 9,0%, průměrné věkové rozmezí 37,3 až 41,9 let, průměrné trvání diabetu bylo 15,5 až 19,2 let a průměrné rozmezí BMI 25,0 až 26,8 kg / m2. Do existujících inzulínových terapií byl přidán Symlin nebo placebo.
Tabulka 3 shrnuje složené výsledky z těchto studií u pacientů přiřazených k dávce 30 nebo 60 mcg po 6 měsících léčby.
Tabulka 3: Průměrná (SE) změna v HbA1c, hmotnosti a inzulínu po 6 měsících ve dvojitě slepých, placebem kontrolovaných studiích u pacientů s diabetem 1. typu
| Proměnná | Placebo | Symlin (30 nebo 60 mcg) |
|---|---|---|
| Výchozí hodnota HbA1c (%) | 9.0 (0.06) | 8.9 (0.04) |
| Změna HbA1c po 6 měsících ve srovnání s výchozím stavem (%) | −0.10 (0.05) | −0.43 (0.04)* |
| Placebem odečtená změna HbA1c po 6 měsících (%) | NA | −0.33 (0.06)* |
| Základní hmotnost (kg) | 75.1 (0.6) | 76.1 (0.5) |
| Změna hmotnosti po 6 měsících ve srovnání s výchozím stavem (kg) | +0.6 (0.1) | −1.1 (0.1)* |
| Změna hmotnosti odečtená podle placeba po 6 měsících (kg) | NA | −1.7 (0.1)* |
| Procentní změna inzulínových dávek po 6 měsících: rychlé / krátkodobé působení | +1.7 (3.3) | −3.6 (2.9) |
| Procentní změna inzulínových dávek po 6 měsících: dlouhodobě působící | +2.5 (1.9) | +1.9 (1.3) |
|
* Statisticky významné snížení ve srovnání s placebem (p-hodnota <0,05). |
V kohortě 73 pacientů, kteří dokončili dva roky léčby Symlinem, byly odečteny základní hodnoty HbA1c a změny hmotnosti: 0,35%, respektive 0,60 kg.
Symlinova dávka-titrační zkouška
U pacientů s diabetem 1. typu byla provedena studie titrace dávky Symlin. Pacienti s relativně dobrou výchozí glykemickou kontrolou (průměr HbA1c = 8,1%) byli randomizováni, aby dostávali buď inzulín plus placebo nebo inzulín plus Symlin. Dalšími výchozími a demografickými charakteristikami byly: průměrný věk 41 let, průměrné trvání diabetu 20 let, průměrný BMI 28 kg / m2. Symlin byl zahájen v dávce 15 mcg a titrován vzestupně v týdenních intervalech po 15 mcg k dávkám 30 mcg nebo 60 mcg, podle toho, zda se u pacientů vyskytla nevolnost. Jakmile bylo dosaženo tolerované dávky 30 mcg nebo 60 mcg, zůstala dávka Symlin po zbytek studie zachována (Symlin byl podán před hlavním jídlem). Během titrace Symlin byla dávka inzulínu (většinou krátce / rychle působící inzulín) snížena o 30-50%, aby se snížil výskyt hypoglykémie. Jakmile byla dosažena tolerovaná dávka Symlinu, byla dávka inzulínu upravena podle standardní klinické praxe na základě monitorování hladiny glukózy v krvi před jídlem a po jídle. Do 6 měsíců léčby měli pacienti léčení Symlinem a inzulínem a pacienti léčení inzulínem a placebem ekvivalentní snížení průměrného HbA1c (0,47 ± 0,07% vs. - 0,49 ± 0,07%, v tomto pořadí); pacienti se Symlinem zhubli („0,33 ± 0,31 kg ve srovnání s výchozím stavem a 2,62 kg ve srovnání s placebem plus pacienty léčenými inzulínem). Pacienti léčení Symlinem používali méně celkového inzulínu (11,7% vzhledem k výchozímu stavu) a méně krátce / rychle působícího inzulínu (22,8%) vzhledem k výchozímu stavu.
Otevřená studie v prostředí klinické praxe
Otevřená studie Symlin byla provedena u pacientů s diabetem typu 1, kteří nebyli schopni dosáhnout glykemických cílů pomocí samotného inzulínu. Po dokončení titrace Symlinu byl u těchto pacientů použit režim inzulinu s flexibilní dávkou (viz DÁVKOVÁNÍ A PODÁNÍ). V této studii pacienti upravovali svůj inzulinový režim na základě monitorování glukózy před jídlem a po jídle. Na začátku studie byl průměrný HbA1c 8,0%, průměrný věk byl 42,7 let, průměrné trvání diabetu bylo 21,2 let a průměrný BMI byl 28,6 kg / m2. Denní dávka přípravku Symlin byla 30 mcg nebo 60 mcg u hlavních jídel.
Symlin plus inzulín snížil HbA1c a tělesnou hmotnost ze základní hodnoty v 6 měsících v průměru o 0,18%, respektive 3,0 kg. Těchto změn v glykemické kontrole a tělesné hmotnosti bylo dosaženo snížením dávek celkem, krátkodobě působící a dlouhodobě působící inzulín („12,0 ± 1,36,“ 21,7 ± 2,81 a „0,4 ± 1,59%), ).
horní
Indikace a použití
Symlin se podává při jídle a je indikován pro:
- Diabetes typu 1, jako doplňková léčba u pacientů, kteří používají inzulínovou terapii před jídlem a kteří nedosáhli požadované regulace glukózy navzdory optimální inzulínové terapii.
- Diabetes 2. typu, jako doplňková léčba u pacientů, kteří používají inzulínovou terapii během jídla a kteří nedosáhli požadovaná regulace glukózy navzdory optimální inzulínové terapii, s nebo bez současného sulfonylmočovinového činidla a / nebo metformin.
horní
Kontraindikace
Symlin je kontraindikován u pacientů s některým z následujících stavů:
- známá přecitlivělost na Symlin nebo na kteroukoli jeho složku, včetně metakresolu;
- potvrzená diagnóza gastroparézy;
- hypoglykémie neznalost.
horní
Varování
Výběr pacienta
Správný výběr pacientů je rozhodující pro bezpečné a efektivní používání Symlin
Před zahájením léčby by měl být zkontrolován HbA1c pacienta, nejnovější údaje o sledování hladiny glukózy v krvi, anamnéza hypoglykémie vyvolané inzulínem, aktuální režim inzulínu a tělesná hmotnost. Léčba Symlinem by měla být zvažována pouze u pacientů s cukrovkou typu 2 nebo typu 1, kteří splňují následující kritéria:
- nedosáhli dostatečné kontroly glykémie navzdory individuálnímu řízení inzulínu;
- dostávají trvalou péči pod vedením zdravotnického odborníka v oblasti užívání inzulínu a jsou podporovány službami pedagoga (ů) cukrovky.
Pacienti, kteří splňují některá z následujících kritérií, by NEMěli být považováni za léčbu Symlinem:
- špatné dodržování současného inzulínového režimu;
- špatné dodržování předepsaného sledování krevní glukózy;
- mají HbA1c> 9%;
- opakující se závažná hypoglykémie vyžadující pomoc během posledních 6 měsíců;
- přítomnost hypoglykémie nevědomosti;
- potvrzená diagnóza gastroparézy;
- vyžadují použití léků, které stimulují gastrointestinální motilitu;
- dětští pacienti.
Hypoglykémie
Samotný Symlin nezpůsobuje hypoglykémii. Je však naznačeno, že Symlin je podáván současně s inzulínovou terapií a v tomto nastavení Symlin zvyšuje riziko inzulínem vyvolané těžké hypoglykémie, zejména u pacientů s typem 1 cukrovka. Těžká hypoglykémie spojená se Symlinem se objevuje během prvních 3 hodin po injekci Symlinu. Dojde-li k závažné hypoglykémii při provozu motorového vozidla, těžkých strojů nebo při provádění jiných vysoce rizikových činností, může dojít k vážným zraněním. Proto při zavádění léčby Symlinem je třeba přijmout vhodná opatření, aby se zabránilo zvyšování rizika těžké hypoglykémie vyvolané inzulínem. Tato opatření zahrnují časté monitorování glukózy před jídlem a po jídle v kombinaci s počátečním snížením dávek krátkodobě působícího inzulínu před jídlem o 50% (viz DÁVKOVÁNÍ A PODÁNÍ).
Mezi příznaky hypoglykémie patří hlad, bolest hlavy, pocení, třes, podrážděnost nebo obtížné soustředění. Rychlé příznaky koncentrace glukózy v krvi mohou takové příznaky vyvolat bez ohledu na hodnoty glukózy. Závažnějšími příznaky hypoglykémie jsou ztráta vědomí, kóma nebo záchvaty.
Včasné varovné příznaky hypoglykémie se mohou za určitých podmínek, jako je dlouhé trvání diabetu, lišit; onemocnění diabetických nervů; použití léků, jako jsou beta-blokátory, klonidin, guanethidin nebo reserpin; nebo zesílená kontrola diabetu.
Přidání jakéhokoli antihyperglykemického činidla, jako je Symlin, do existujícího režimu jednoho nebo více antihyperglykemických látek (např. Inzulínu, sulfonylmočoviny) nebo jiné látky, které mohou zvýšit riziko hypoglykémie, mohou vyžadovat další úpravu dávky inzulínu a zvláště pečlivé sledování hladiny glukózy v krvi.
Níže jsou uvedeny příklady látek, které mohou zvýšit účinek na snížení hladiny glukózy v krvi a náchylnost k hypoglykémii: orální antidiabetika produkty, ACE inhibitory, diisopyramid, fibráty, fluoxetin, MAO inhibitory, pentoxifylin, propoxyfen, salicyláty a sulfonamid antibiotika.
Klinické studie využívající kontrolovanou hypoglykemickou výzvu prokázaly, že Symlin nemění protiregulační hormonální odpověď na hypoglykémii indukovanou inzulínem. Podobně u pacientů léčených Symlinem se vnímání hypoglykemických příznaků nezměnilo s koncentracemi glukózy v plazmě tak nízkými jako 45 mg / dl.
horní
Opatření
Všeobecné
Hypoglykémie (viz VAROVÁNÍ).
Symlin by měl být předepsán s opatrností osobám se zrakovým nebo obratovým postižením.
Informace pro pacienty
Poskytovatelé zdravotní péče by měli informovat pacienty o možných rizicích a výhodách léčby Symlinem. Poskytovatelé zdravotní péče by měli také informovat pacienty o postupech samosprávy, včetně monitorování glukózy, správné techniky injekce, načasování dávkování a správného skladování Symlin. Dále posílit důležitost dodržování plánování jídla, fyzické aktivity, rozpoznávání a řízení hypoglykémie a hyperglykémie a hodnocení komplikací diabetu. Další informace naleznete v Příručce k medikaci Symlin a Pokyny pro použití pacienta.
Poučte pacienty o řešení zvláštních situací, jako jsou interkurentní stavy (nemoc nebo stres), neadekvátní nebo vynechaná dávka inzulínu, neúmyslné podání zvýšené dávky inzulínu nebo Symlin, nedostatečný příjem potravy nebo zmeškání jídla.
Symlin a inzulín by měly být vždy podávány jako samostatné injekce a nikdy nemíchány.
Ženy s diabetem by měly být informovány, aby informovaly svého zdravotnického pracovníka, pokud jsou těhotné nebo uvažují o těhotenství.
Renální postižení
Požadavky na dávkování přípravku Symlin se u pacientů se středně těžkou nebo těžkou poruchou funkce ledvin (ClCr> 20 až ± 50 ml / min) nemění. U dialyzovaných pacientů nebyly provedeny žádné studie (viz KLINICKÁ FARMAKOLOGIE; Zvláštní populace).
Jaterní postižení
Studie u pacientů s poškozením jater nebyly provedeny. Neočekává se však, že by jaterní dysfunkce ovlivňovala koncentraci Symlinu v krvi (viz KLINICKÁ FARMAKOLOGIE; Zvláštní populace).
Alergie
Místní alergie
U pacientů může dojít k zarudnutí, otoku nebo svědění v místě vpichu. Tyto drobné reakce obvykle ustoupí během několika dní až několika týdnů. V některých případech mohou tyto reakce souviset s jinými faktory, než je Symlin, jako jsou dráždivé látky v přípravku na čištění kůže nebo nesprávná technika injekce.
Systémová alergie
V kontrolovaných klinických studiích do 12 měsíců byly potenciální systémové alergické reakce hlášeny u 65 (5%) pacientů typu 2 a 59 (5%) pacientů léčených Symlinem typu 1. Podobné reakce byly hlášeny 18 (4%) a 28 (5%) pacientů léčených placebem 2. typu a 2. typu. Žádný pacient, který obdržel Symlin, nebyl ze studie odebrán kvůli možné systémové alergické reakci.
Lékové interakce
Vzhledem k jeho účinkům na vyprazdňování žaludku by neměla být terapie Symlinem zvažována u pacientů užívajících léky, které mění gastrointestinální trakt pohyblivost (např. anticholinergická činidla, jako je atropin) a činidla, která zpomalují intestinální absorpci živin (např. Î ± glukosidáza) inhibitory). Pacienti užívající tyto léky nebyli v klinických studiích studováni.
Symlin má potenciál zpomalit absorpci souběžně podávaných perorálních léků. Pokud je rychlý nástup souběžně podávaného perorálně podávaného činidla kritickým určujícím činitelem účinnosti (jako jsou analgetika), by mělo být činidlo podáváno alespoň 1 hodinu před Symlinem nebo 2 hodiny po něm injekce.
V klinických studiích současné užívání sulfonylmočovin nebo biguanidů nezměnilo profil nežádoucích účinků přípravku Symlin. Nebyly provedeny žádné formální studie interakcí, které by posoudily účinek přípravku Symlin na kinetiku perorálních antidiabetik.
Míchání Symlin a Insulin
Farmakokinetické parametry Symlinu byly změněny, když byly smíchány s běžnými, NPH a 70/30 předem smísenými formulacemi rekombinantního lidského inzulínu bezprostředně před injekcí. Symlin a inzulín by proto neměly být míchány a musí být podávány samostatně.
Karcinogeneze, mutageneze, zhoršení plodnosti
Karcinogeneze
U myší CD-1 byla provedena dvouletá studie karcinogenity s dávkami Symlin 0,2, 0,5 a 1,2 mg / kg / den (32, 67 a 159krát) expozice vyplývající z maximální doporučené dávky pro člověka na základě plochy pod křivkou plazmatické koncentrace nebo AUC, ). Nebyly pozorovány žádné nádory vyvolané léky. U potkanů Sprague-Dawley byla provedena dvouletá studie karcinogenity s dávkami 0,04, 0,2 a 0,5 mg / kg / den Symlin (3, 9 a 25násobek expozice vyplývající z maximální doporučené dávky pro člověka na základě AUC, ). U žádného orgánu nebyly pozorovány žádné nádory vyvolané léky.
Mutageneze
Symlin nebyl v Amesově testu mutagenní a v testu lidských lymfocytů nezvýšil chromozomální aberaci. Symlin nebyl klastogenní v in vivo testu na myších mikronukleech nebo v testu chromozomální aberace využívající ovariální buňky čínského křečka.
Snížení plodnosti
Podávání Symlin 0,3, 1 nebo 3 mg / kg / den (8, 17 a 82násobek expozice vyplývající z maxima doporučená dávka pro člověka podle plochy povrchu těla) neměla významný vliv na plodnost u mužů nebo žen krysy. Nejvyšší dávka 3 mg / kg / den měla za následek dystokii u 8/12 samic potkanů sekundárně k významnému snížení hladin vápníku v séru.
Těhotenství
Teratogenní účinky: Těhotenství Kategorie C
U těhotných žen nebyly provedeny žádné adekvátní a dobře kontrolované studie. Studie na perfundované lidské placentě naznačují, že Symlin má nízký potenciál prostupovat placentární bariérou matky / plodu. U potkanů a králíků byly provedeny studie embryofetální toxicity se Symlinem. Zvýšení vrozených abnormalit (defekt nervové trubice, rozštěp patra, exencefalie) bylo pozorováno u plodů potkanů léčených během organogeneze s 0,3 a 1,0 mg / kg / den (10 a 47násobek expozice vyplývající z maximální doporučené dávky pro člověka na základě AUC, ). Podávání dávek až do 0,3 mg / kg / den Symlin (9krát maximální doporučená dávka na základě AUC) těhotným králíkům nemělo žádné nepříznivé účinky na embryofetální vývoj; studie reprodukce na zvířatech však ne vždy predikují lidskou odpověď. Přípravek Symlin by měl být používán během těhotenství, pouze pokud je podle zdravotnického personálu stanoveno, že potenciální přínos odůvodňuje možné riziko pro plod.
Kojící matky
Není známo, zda se Symlin vylučuje do mateřského mléka. Mnoho léčiv, včetně peptidových, se vylučuje do mateřského mléka. Proto by měl být přípravek Symlin podáván kojícím ženám pouze tehdy, pokud je podle zdravotnického personálu stanoveno, že potenciální přínos převažuje nad potenciálním rizikem pro kojence.
Pediatrické použití
Bezpečnost a účinnost přípravku Symlin u pediatrických pacientů nebyla stanovena.
Geriatrické použití
Přípravek Symlin byl zkoumán u pacientů ve věku od 15 do 84 let, včetně 539 pacientů ve věku 65 let a starších. Změna hodnot HbA1c a frekvence hypoglykémie se nelišila podle věku, ale u některých starších jedinců nelze vyloučit vyšší citlivost. Proto by režimy Symlin i inzulín měly být pečlivě zvládnuty, aby se předešlo zvýšenému riziku těžké hypoglykémie.
horní
Nežádoucí reakce
Nežádoucí účinky (kromě hypoglykémie, diskutované níže), které jsou běžně spojeny se Symlinem při současném podávání s fixní dávkou inzulínu dlouhodobé, placebem kontrolované studie u pacientů užívajících inzulín typu 2 a pacientů typu 1 jsou uvedeny v tabulce 4 a 5, resp. Stejné nežádoucí účinky byly také ukázány v otevřené klinické studii klinické praxe, která využívala flexibilní dávkování inzulínu.
Tabulka 4: Naléhavé nežádoucí příhody, které se vyskytují s 5% incidencí a větší incidencí s Symlinem ve srovnání s placebem v dlouhodobých, placebem kontrolovaných pokusech. Výskyt stejných událostí ve studii otevřené klinické praxe (pacienti s diabetem typu 2 užívajícím inzulín, 120 mcg)
| Dlouhodobá, placebem kontrolovaná studia | Open-Label, Clinical Practice Study | ||
|---|---|---|---|
| Placebo + inzulín (n (%)) (N = 284) |
Symlin + inzulín (n (%)) (N = 292) |
Symlin + inzulín (n (%)) (N = 166) |
|
| Nevolnost | 34 (12) | 81 (28) | 53 (30) |
| Bolest hlavy | 19 (7) | 39 (13) | 8 (5) |
| Anorexie | 5 (2) | 27 (9) | 1 (<1) |
| Zvracení | 12 (4) | 24 (8) | 13 (7) |
| Bolest břicha | 19 (7) | 23 (8) | 3 (2) |
| Únava | 11 (4) | 20 (7) | 5 (3) |
| Závrať | 11 (4) | 17 (6) | 3 (2) |
| Kašel | 12 (4) | 18 (6) | 4 (2) |
| Zánět hltanu | 7 (2) | 15 (5) | 6 (3) |
Tabulka 5: Naléhavé nežádoucí příhody, které se vyskytují s 5% incidencí a větší incidencí se Symlinem ve srovnání s placebem v dlouhodobých, placebem kontrolovaných studiích. Výskyt stejných událostí ve studii otevřené klinické praxe (pacienti s diabetem 1. typu, 30 nebo 60 mcg)
| Dlouhodobá, placebem kontrolovaná studia | Open-Label, Clinical Practice Study | ||
|---|---|---|---|
| Placebo + inzulín (n (%)) (N = 538) |
Symlin + inzulín (n (%)) (N = 716) |
Symlin + inzulín (n (%)) (N = 265) |
|
| Nevolnost | 92 (17) | 342 (48) | 98 (37) |
| Anorexie | 12 (2) | 122 (17) | 0 (0) |
| Zranění | 55 (10) | 97 (14) | 20 (8) |
| Zvracení | 36 (7) | 82 (11) | 18 (7) |
| Arthralgia | 27 (5) | 51 (7) | 6 (2) |
| Únava | 22 (4) | 51 (7) | 12 (4.5) |
| Alergická reakce | 28 (5) | 41 (6) | 1 (<1) |
| Závrať | 21 (4) | 34 (5) | 5 (2) |
Většina nežádoucích účinků byla gastrointestinální povahy. U pacientů s diabetem 2. nebo 1. typu byl výskyt nauzey na začátku léčby Symlinem vyšší a u většiny pacientů časem klesal. Incidence a závažnost nevolnosti jsou sníženy, když je Symlin postupně titrován na doporučené dávky (viz DÁVKOVÁNÍ A PODÁNÍ).
Těžká hypoglykémie
Samotný Symlin (bez současného podávání inzulínu) nezpůsobuje hypoglykémii. Symlin je však indikován jako doplňková léčba u pacientů, kteří používají inzulínovou terapii při jídle a současné podávání Symlin s inzulínem může zvýšit riziko hypoglykémie vyvolané inzulínem, zejména u pacientů s diabetem 1. typu (vidět Varování v krabici). Výskyt těžké hypoglykémie během programu klinického vývoje Symlin je shrnut v tabulce 6 a tabulce 7.
Tabulka 6: Incidence a rychlost výskytu těžké hypoglykémie u dlouhodobých, placebem kontrolovaných a otevřených štítků, klinické studie u pacientů s diabetem typu 2 užívajícím inzulín
| Dlouhodobý, Placebo-kontrolované studie (Během zahájení léčby nedošlo ke snížení dávky inzulínu) |
Otevřený, Studie klinické praxe (Snížení dávky inzulínu během zahájení léčby) |
|||||
|---|---|---|---|---|---|---|
| Placebo + inzulín | Symlin + inzulín | Symlin + inzulín | ||||
|
Těžká hypoglykémie |
0-3 Měsíce (n = 284) |
>3-6 Měsíce (n = 251) |
0-3 Měsíce (n = 292) |
>3-6 Měsíce (n = 255) |
0-3 Měsíce (n = 166) |
>3-6 Měsíce (n = 150) |
| Zjištěno pacientem * | ||||||
| Míra události (míra události / rok pacienta) | 0.24 | 0.13 | 0.45 | 0.39 | 0.05 | 0.03 |
| Incidence (%) | 2.1 | 2.4 | 8.2 | 4.7 | 0.6 | 0.7 |
| Lékařsky asistované - | ||||||
| Míra události (míra události / rok pacienta) | 0.06 | 0.07 | 0.09 | 0.02 | 0.05 | 0.03 |
| Incidence (%) | 0.7 | 1.2 | 1.7 | 0.4 | 0.6 | 0.7 |
|
* Vážná hypoglykémie zjištěná pacientem: Vyžaduje pomoc jiného jedince (včetně pomoci při požití perorálního uhlohydrátu); a / nebo vyžadující podání injekce glukagonu, intravenózní glukózy nebo jiného lékařského zákroku. - Zdravotně asistovaná těžká hypoglykémie: Vyžadování glukagonu, IV glukózy, hospitalizace, zdravotnická pomoc, návštěva pohotovostní místnosti a / nebo vyšetřovatelem je hodnocena jako SAE. |
Tabulka 7: Incidence a míra výskytu těžké hypoglykémie u dlouhodobých, placebem kontrolovaných a otevřených štítků, klinické studie u pacientů s diabetem 1. typu
| Dlouhodobý, Placebo-kontrolované studie (Během zahájení léčby nedošlo ke snížení dávky inzulínu) |
Otevřený, Studie klinické praxe (Snížení dávky inzulínu během zahájení léčby) |
|||||
|---|---|---|---|---|---|---|
| Placebo + inzulín | Symlin + inzulín | Symlin + inzulín | ||||
|
Těžká hypoglykémie |
0-3 Měsíce (n = 538) |
>3-6 Měsíce (n = 470) |
0-3 Měsíce (n = 716) |
>3-6 Měsíce (n = 576) |
0-3 Měsíce (n = 265) |
>3-6 Měsíce (n = 213) |
| Zjištěno pacientem * | ||||||
| Míra události (míra události / rok pacienta) | 1.33 | 1.06 | 1.55 | 0.82 | 0.29 | 0.16 |
| Incidence (%) | 10.8 | 8.7 | 16.8 | 11.1 | 5.7 | 3.8 |
| Lékařsky asistované - | ||||||
| Míra události (míra události / rok pacienta) | 0.19 | 0.24 | 0.50 | 0.27 | 0.10 | 0.04 |
| Incidence (%) | 3.3 | 4.3 | 7.3 | 5.2 | 2.3 | 0.9 |
|
* Vážná hypoglykémie zjištěná pacientem: Vyžaduje pomoc jiného jedince (včetně pomoci při požití perorálního uhlohydrátu); a / nebo vyžadující podání injekce glukagonu, intravenózní glukózy nebo jiného lékařského zákroku. - Zdravotně asistovaná těžká hypoglykémie: Vyžadování glukagonu, IV glukózy, hospitalizace, zdravotnická pomoc, návštěva pohotovostní místnosti a / nebo vyšetřovatelem je hodnocena jako SAE. |
Zkušenosti po uvedení na trh
Od uvedení na trh společnosti Symlin byly hlášeny následující nežádoucí účinky. Protože tyto události jsou hlášeny dobrovolně z populace nejisté velikosti, není vždy možné spolehlivě odhadnout jejich frekvenci nebo navázat příčinnou souvislost s expozicí lékům.
Obecně: Reakce v místě vpichu.
Předávkovat
Jednorázové dávky 10 mg Symlinu (83násobek maximální dávky 120 mcg) byly podány třem zdravým dobrovolníkům. U všech tří jedinců byla hlášena těžká nevolnost a byla spojena s zvracením, průjmem, vazodilatací a závratěmi. Nebyla hlášena žádná hypoglykémie. Symlin má krátký poločas a v případě předávkování jsou uvedena podpůrná opatření.
horní
Dávkování a správa
Dávka Symlin se liší v závislosti na tom, zda má pacient diabetes 2. nebo 1. typu (viz níže). Při zahájení léčby přípravkem Symlin je nutné snížit počáteční dávku inzulinu u všech pacientů (typu 2 i typu 1), aby se snížilo riziko hypoglykémie vyvolané inzulínem. Protože toto snížení inzulinu může vést ke zvýšení hladiny glukózy, je třeba pacienty v pravidelných intervalech sledovat posoudit snášenlivost Symlin a účinek na hladinu glukózy v krvi, aby bylo možné provést individuální přizpůsobení inzulínu zahájeno. Pokud je léčba Symlinem z jakéhokoli důvodu přerušena (např. Chirurgický zákrok nebo onemocnění), měl by být při opětovném zahájení terapie Symlinem dodržen stejný iniciační protokol (viz níže).
Zahájení terapie Symlinem
Pacienti s diabetem typu 2 užívajícím inzulín
U pacientů s diabetes mellitus 2. typu by měl být Symlin zahájen dávkou 60 mcg a podle tolerance by měl být zvýšen na dávku 120 mcg.
Pacienti by měli být poučeni, aby:
- Inicioval Symlin při 60 mcg subkutánně, bezprostředně před hlavním jídlem;
- Snižte preprandiální, rychle působící nebo krátkodobě působící dávky inzulínu, včetně inzulínů s pevnou směsí (70/30), o 50%;
- Monitorujte hladinu glukózy v krvi často, včetně před a po jídle a před spaním;
- Pokud nedojde ke klinicky významné nevolnosti po dobu 3-7 dnů, zvyšte dávku Symlin na 120 mcg. Úprava dávky Symlin by měla být prováděna pouze podle pokynů lékaře. Pokud významná nevolnost přetrvává při dávce 120 mcg, dávka Symlinu by měla být snížena na 60 mcg;
- Jakmile je dosaženo cílové dávky Symlinu a nevolnosti (pokud se vyskytne), upravte dávky inzulínu, aby se optimalizovala glykemická kontrola. Úprava dávky inzulínu by měla být prováděna pouze podle pokynů lékaře;
- Chcete-li zkontrolovat alespoň Symlin a upravit dávku inzulinu, obraťte se na zdravotnického odborníka v používání inzulínu jednou týdně, dokud není dosaženo cílové dávky Symlin, je Symlin dobře snášen a koncentrace glukózy v krvi jsou stabilní.
Pacienti s diabetem 1. typu
U pacientů s diabetem 1. typu by měl být Symlin zahájen dávkou 15 mcg a titrován v přírůstcích 15 mcg na udržovací dávku 30 mcg nebo 60 mcg, jak je tolerováno.
Pacienti by měli být poučeni, aby:
- Zahajte Symlin počáteční dávkou 15 mcg subkutánně, bezprostředně před hlavním jídlem;
- Snižte preprandiální, rychle působící nebo krátkodobě působící dávky inzulínu, včetně inzulínů s fixní směsí (např. 70/30) o 50%;
- Monitorujte hladinu glukózy v krvi často, včetně před a po jídle a před spaním;
- Zvýšte dávku Symlin na další přírůstek (30 mcg, 45 mcg nebo 60 mcg), pokud po dobu nejméně 3 dnů nedošlo k žádné klinicky významné nevolnosti. Úprava dávky Symlin by měla být prováděna pouze podle pokynů lékaře. Pokud významná nevolnost přetrvává při dávce 45 nebo 60 mcg, dávka Symlinu by měla být snížena na 30 mcg. Pokud dávka 30 mcg není tolerována, mělo by se zvážit přerušení léčby Symlinem;
- Jakmile je dosaženo cílové dávky Symlinu a nevolnosti (pokud se vyskytne), upravte dávky inzulínu, aby se optimalizovala glykemická kontrola. Úprava dávky inzulínu by měla být prováděna pouze podle pokynů lékaře;
- Chcete-li zkontrolovat alespoň Symlin a upravit dávku inzulinu, obraťte se na zdravotnického odborníka v používání inzulínu jednou týdně, dokud není dosaženo cílové dávky Symlin, je Symlin dobře snášen a koncentrace glukózy v krvi jsou stabilní.
Jakmile je u pacientů typu 2 nebo typu 1 dosaženo cílové dávky Symlin
Po dosažení udržovací dávky přípravku Symlin by pacienti s diabetem typu 2 i pacienti s diabetem typu 1 měli být poučeni, aby:
- Jakmile je dosaženo cílové dávky Symlinu a nevolnosti (pokud se vyskytne), upravte dávky inzulínu, aby se optimalizovala glykemická kontrola. Úprava dávky inzulínu by měla být prováděna pouze podle pokynů lékaře;
- V případě opakované nauzey nebo hypoglykémie kontaktujte lékaře. Zvýšená četnost mírné až střední hypoglykémie by měla být vnímána jako varovný signál zvýšeného rizika těžké hypoglykémie.
Správa
Symlin by měl být podáván subkutánně bezprostředně před každým hlavním jídlem (¥ ¥ 250 kcal nebo obsahujícím g 30 g uhlohydrátů).
Před podáním by měl být přípravek Symlin při pokojové teplotě, aby se snížily možné reakce v místě vpichu. Každá dávka přípravku Symlin by měla být podávána subkutánně do břicha nebo stehna (podávání do paže se nedoporučuje kvůli variabilní absorpci). Místa vpichu by se měla otáčet, aby se stejné místo nepoužívalo opakovaně. Vybrané místo vpichu by mělo být také odlišné od místa vybraného pro jakoukoli souběžnou injekci inzulínu.
- Symlin a inzulín by měly být vždy podávány jako samostatné injekce.
- Symlin by neměl být mísen s žádným typem inzulínu.
- Pokud dojde k vynechání dávky Symlin, počkejte na další plánovanou dávku a podejte obvyklé množství.
Injekční pero SymlinPen®
Pero injektor SymlinPen® je k dispozici ve dvou prezentacích:
- Pero injekční stříkačka SymlinPen® 60 pro dávky 15 mcg, 30 mcg, 45 mcg, 60 mcg.
- Pero injekční stříkačka SymlinPen® 120 pro dávky 60 mcg a 120 mcg.
Pokyny k použití injekčního pera SymlinPen® naleznete v přiloženém návodu k použití pacienta.
Pacient by měl být poučen:
- k potvrzení, že používají správný injektor pera, který dodá jejich předepsanou dávku;
- o správném použití injektoru pera, s důrazem na to, jak a kdy nastavit nový injektor na pero;
- nepřenášet Symlin z injekčního pera do injekční stříkačky. Mohlo by to vést k vyšší dávce, než bylo zamýšleno, protože Symlin v injekčním peru je vyšší koncentrace než Symlin v injekční lahvičce Symlin;
- nesdílet injekční pero a jehly s ostatními;
- že jehly nejsou součástí injektoru pera a musí být zakoupeny samostatně;
- která délka a průměr jehly by měly být použity;
- použít novou jehlu pro každou injekci.
Lahvičky Symlin
K podání Symlin z lahviček použijte pro optimální přesnost inzulínovou stříkačku U-100 (nejlépe 0,3 ml [0,3 cc]). Pokud používáte stříkačku kalibrovanou pro použití s inzulínem U-100, použijte níže uvedenou tabulku (tabulka 8) k měření dávky mikrogramu v jednotkových krocích.
Tabulka 8: Převod dávky Symlin na ekvivalenty inzulínových jednotek
| Předepsané dávkování (mcg) | Přírůstek pomocí stříkačky U-100 (jednotky) | Objem (cc nebo mL) |
|---|---|---|
| 15 | 2 ½ | 0.025 |
| 30 | 5 | 0.05 |
| 45 | 7 ½ | 0.075 |
| 60 | 10 | 0.1 |
| 120 | 20 | 0.2 |
K injekcím Symlin a inzulínu vždy používejte samostatné nové stříkačky a jehly.
Přerušení léčby
Terapie Symlinem by měla být přerušena, pokud nastane některá z následujících situací:
* Opakující se nevysvětlitelná hypoglykémie, která vyžaduje lékařskou pomoc;
* Trvalá klinicky významná nevolnost;
* Nesoulad s vlastním monitorováním koncentrací glukózy v krvi;
* Nesoulad s úpravou dávky inzulínu;
* Nesoulad s plánovanými kontakty zdravotnického personálu nebo doporučenými návštěvami kliniky.
Příprava a manipulace
Symlin by měl být před podáním vizuálně zkontrolován, zda neobsahuje částice nebo zda nedošlo ke změně barvy, kdykoli to roztok a nádoba dovolí.
horní
Jak dodáván
Symlin je dodáván jako sterilní injekce v následujících lékových formách:
- 1,5 ml jednorázové injekční pero SymlinPen® 60 na jedno použití obsahující 1 000 mcg / ml pramlintidu (jako acetát).
- 2,7 ml jednorázové injekční pero SymlinPen® 120 pro pero, obsahující 1 000 mcg / ml pramlintidu (jako acetát).
- 5 ml lahvička, obsahující 600 mcg / ml pramlintidu (jako acetát), pro použití s inzulínovou stříkačkou.
K podání Symlin z lahviček použijte inzulínovou stříkačku U-100 (s výhodou 0,3 ml [0,3 cc]). Pokud používáte stříkačku kalibrovanou pro použití s inzulínem U-100, použijte tabulku (tabulka 8) v tabulce DÁVKOVÁNÍ A PODÁNÍ Sekce pro měření dávky mikrogramů v jednotkových krocích.
Nemíchejte přípravek Symlin s inzulínem.
Aplikace Symlin Injection je k dispozici v následujících velikostech balení:
- Pero injektor SymlinPen® 60, obsahující 1 000 mcg / ml pramlintidu (jako acetát)
2 x 1,5 ml jednorázové injekční pero s více dávkami
(NDC 66780-115-02) - Pero injekční stříkačka SymlinPen® 120 obsahující 1 000 mcg / ml pramlintidu (jako acetát)
2 x 2,7 ml jednorázové injekční pero s více dávkami
(NDC 66780-121-02) - 5 ml lahvička, obsahující 600 mcg / ml pramlintidu (jako acetát), pro použití s inzulínovou stříkačkou
(NDC 66780-110-01)
Úložný prostor
Nepoužívané injekční stříkačky a injekční lahvičky Symlin: Chlazení (36 ° F až 46 ° F; 2 ° C až 8 ° C) a chraňte před světlem. Chraňte před mrazem. Nepoužívejte, pokud byl produkt zmrazený. Nepoužitý Symlin (otevřený nebo neotevřený) by neměl být používán po uplynutí doby použitelnosti (EXP) vytištěné na krabičce a na štítku.
Používané injekční stříkačky a injekční lahvičky Symlin: Po prvním použití chladit nebo uchovávat po dobu 30 dnů při teplotě nepřesahující 30 ° C. Spotřebujte do 30 dnů, v chladu nebo ne.
Podmínky skladování jsou shrnuty v tabulce 9.
Tabulka 9: Podmínky skladování
| Dávkovači forma | Neotevřené (nepoužívá se) Chlazené |
Otevřeno (v provozu) Chlazené nebo Teplota Až 30 ° C |
|---|---|---|
| 1,5 ml injekčního pera 2,7 ml injekční pero 5 ml lahvička |
Do data expirace | Spotřebujte do 30 dnů |
Pero injekční stříkačky a injekční lahvičky SymlinPen® jsou vyráběny pro: Amylin Pharmaceuticals, Inc. San Diego, CA 92121 USA 1-800-349-8919 http://www.Symlin.com
Pouze Rx
Značka Symlin, designová značka Symlin a SymlinPen jsou registrované ochranné známky společnosti Amylin Pharmaceuticals, Inc. Copyright © 2005-2008, Amylin Pharmaceuticals, Inc. Všechna práva vyhrazena.
Poslední aktualizace: červenec 2008
Symlin, Symlin Pen, pramlintide acetát, informace o pacientech
Účelem informací v této monografii není pokrýt všechna možná použití, pokyny, preventivní opatření, lékové interakce nebo nepříznivé účinky. Tyto informace jsou zobecněné a neslouží jako zvláštní lékařská pomoc. Pokud máte dotazy týkající se léčivých přípravků, které užíváte, nebo byste chtěli získat více informací, obraťte se na svého lékaře, lékárníka nebo zdravotní sestru.
zpět k: Procházet všechny léky na cukrovku


